Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
\(4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2\\ 2SO_2 + O_2 \xrightarrow{t^o,xt} 2SO_3\\ SO_3 + H_2O \to H_2SO_4\\ Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O\\ Fe_2(SO_4)_3 + 6KOH \to 2Fe(OH)_3 + 3K_2SO_4\\ Fe_2(SO_4)_3 + 3BaCl_2 \to 3BaSO_4 + 2FeCl_3\)
b)
\(3Mg + 4H_2SO_4 \to 3MgSO_4 + S + 4H_2O\\ S + Mg \xrightarrow{t^o} MgS\\ MgS + 2HCl \to MgCl_2 + H_2S\\ H_2S + \dfrac{1}{2}O_2 \xrightarrow{t^o} S + H_2O\\ S + O_2 \xrightarrow{t^o} SO_2\\ SO_2 + NaOH \to NaHSO_3\\ NaHSO_3 + NaOH \to Na_2SO_3 + H_2O\\ Na_2SO_3 + H_2SO_4 \to Na_2SO_4 + SO_2 + H_2O\\ Na_2SO_4 + BaCl_2 \to BaSO_4 + 2NaCl\)

Đáp án C.
Các chất FeSO4, Ag, Na2SO3.
2FeSO4 + 2H2SO4 → Fe2(SO4)3 + SO2 + 2H2O
2Ag + 2H2SO4 → Ag2SO4 + SO2 + 2H2O
Na2SO3 + H2SO4 → Na2SO4 + SO2 + H2O

a) Trích mẫu thử
Cho dung dịch Ba(OH)2 vào các mẫu thử
- mẫu thử nào tạo kết tủa trắng là H2SO4,Na2SO4. Gọi là nhóm 1
\(H_2SO_4 + Ba(OH)_2 \to BaSO_4 + 2H_2O\\ Na_2SO_4 + Ba(OH)_2 \to BaSO_4 + 2NaOH\)
- mẫu thử nào không hiện tượng là NaCl,HCl.Gọi là nhóm 2
Cho giấy quỳ tím lần lượt vào mẫu thử nhóm 1 và 2
Trong nhóm 1 :
- mẫu thử nào làm quỳ tím hóa đỏ là H2SO4
- mẫu thử không hiện tượng là Na2SO4
Trong nhóm 2 :
- mẫu thử nào làm quỳ tím hóa đỏ là HCl
- mẫu thử nào không hiện tượng là NaCl
b)
Trích mẫu thử
Cho quỳ tím vào
- mẫu thử chuyển màu đỏ là HCl
Cho dung dịch Bari clorua vào mẫu thử còn :
- mẫu thử tạo kết tủa trắng là Na2SO4
\(BaCl_2 + Na_2SO_4 \to BaSO_4 + 2NaCl\)
Cho dung dịch bạc nitrat vào mẫu thử còn
- mẫu thử nào tạo kết tủa trắng : KCl
\(KCl + AgNO_3 \to AgCl + KNO_3\)
- mẫu thử không hiện tượng : KNO3
a, _ Trích mẫu thử.
_ Cho một lượng mẫu thử vào ống nghiệm chứa dd Ba(OH)2.
+ Nếu xuất hiện kết tủa trắng, đó là Na2SO4, H2SO4. (1)
PT: \(Ba\left(OH\right)_2+Na_2SO_4\rightarrow2NaOH+BaSO_{4\downarrow}\)
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_{4\downarrow}+2H_2O\)
+ Nếu không có hiện tượng, đó là NaCl, HCl. (2)
_ Nhỏ vài giọt mẫu thử ở cả nhóm (1) và (2) vào giấy quỳ tím.
+ Nếu quỳ tím hóa đỏ thì ở nhóm (1) là H2SO4, nhóm (2) là HCl.
+ Nếu quỳ tím không chuyển màu thì ở nhóm (1) là Na2SO4, nhóm (2) là NaCl.
_ Dán nhãn.
b, _ Trích mẫu thử.
_ Nhỏ 1 lượng từng mẫu thử vao giấy quỳ tím.
+ Nếu quỳ tím hóa đỏ, đó là HCl.
+ Nếu quỳ tím không đổi màu, đó là KCl, KNO3 và Na2SO4. (1)
_ Nhỏ 1 lượng mẫu thử nhóm (1) vào ống nghiệm chứa dd BaCl2.
+ Nếu xuất hiện kết tủa trắng, đó là Na2SO4.
PT: \(BaCl_2+Na_2SO_4\rightarrow2NaCl+BaSO_{4\downarrow}\)
+ Nếu không có hiện tượng, đó là KCl, KNO3. (2)
_ Nhỏ 1 lượng mẫu thử nhóm (2) vào ống nghiệm chứa dd AgNO3.
+ Nếu xuất hiện kết tủa trắng, đó là KCl.
PT: \(KCl+AgNO_3\rightarrow KNO_3+AgCl_{\downarrow}\)
+ Nếu không có hiện tượng, đó là KNO3.
_ Dán nhãn.
Bạn tham khảo nhé!

a)
- Cho các dd tác dụng với quỳ tím:
+ QT chuyển xanh: NaOH
+ QT chuyển đỏ: H2SO4
+ QT không chuyển màu: Na2SO4, NaCl, Na2SO3 (1)
- Cho dd ở (1) tác dụng với dd HCl dư:
+ không hiện tượng: Na2SO4, NaCl (2)
+ Sủi bọt khí: Na2SO3
Na2SO3 + 2HCl --> 2NaCl + SO2 + H2O
- Cho dd ở (2) tác dụng với dd BaCl2:
+ không hiện tượng: NaCl
+ kết tủa trắng: Na2SO4
\(Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
b)
- Cho các dd tác dụng với dd Ba(OH)2
+ Không hiện tượng: HCl
\(Ba\left(OH\right)_2+2HCl\rightarrow BaCl_2+2H_2O\)
+ Kết tủa trắng: H2SO4, Na2SO4, NaHSO3 (1)
\(Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4\downarrow+2H_2O\)
\(Na_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+2NaOH\)
\(Ba\left(OH\right)_2+2NaHSO_3\rightarrow BaSO_3\downarrow+Na_2SO_3+2H_2O\)
- Cho dd ở (1) tác dụng với dd HCl dư:
+ Không hiện tượng: H2SO4, Na2SO4 (2)
+ Sủi bọt khí: NaHSO3
\(NaHSO_3+HCl\rightarrow NaCl+SO_2+H_2O\)
- Cho dd ở (2) tác dụng với quỳ tím:
+ QT chuyển đỏ: H2SO4
+ QT không chuyển màu: Na2SO4
c)
- Cho các dd tác dụng với quỳ tím:
+ QT chuyển đỏ: HCl
+ QT không chuyển màu: NaCl, Na2SO4, Ba(NO3)2 (1)
- Cho dd ở (1) tác dụng với dd BaCl2:
+ không hiện tượng: NaCl, Ba(NO3)2 (2)
+ Kết tủa trắng: Na2SO4
\(Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
- Cho dd ở (2) tác dụng với dd AgNO3
+ Không hiện tượng: Ba(NO3)2
+ Kết tủa trắng: NaCl
\(NaCl+AgNO_3\rightarrow AgCl\downarrow+NaNO_3\)

a) Cu + 2H2SO4 đặc->CuSO4+SO2+2H2O
b) Fe + H2SO4 đặc nguội-> ko pứ
c) 2H2SO4 đặc + S->3SO2+2H2O
d) H2SO4 đặc + KBr-> K2SO4 + Br2 + SO2 + 2H2O
e) H2SO4 đặc nguội + Al-> kopu
g) H2SO4 đặc + FeO->Fe2(SO4)3 + SO2 + H2O
h)4 H2SO4 đặc + 2Fe(OH)2->Fe2(SO4)3 + SO2 +6 H2O
i)6 H2SO4 đặc , dư + 2Fe (t0)->Fe2(SO4)3 +3 SO2 +6 H2O
m) C+ 2H2SO4 đặc-> CO2+2SO2+2H2O
n) H2SO4 đặc + 2NaOH->Na2SO4+2H2O
o) H2SO4 đặc + MgO->MgSO4+H2O
k)3 H2SO4 đặc + Fe2O3->Fe2(SO4)3+3H2O

a)
$FeS + 2HCl \to FeCl_2 + H_2$
$2H_2S + SO_2 \to 3S + 2H_2O$
$S + O_2 \xrightarrow{t^o} SO_2$
$2SO_2 + O_2 \xrightarrow{t^o,xt} 2SO_3$
$SO_3 + H_2O \to H_2SO_4$
$Ba + H_2SO_4 \to BaSO_4 + H_2$
b)
$SO_2 + 2H_2S \to 3S + 2H_2O$
$Fe + S \xrightarrow{t^o} FeS$
$FeS + 2HCl \to FeCl_2 + H_2S$
$H_2S + \dfrac{3}{2} O_2 \xrightarrow{t^o} SO_2 + H_2O$
$SO_2 + 2NaOH \to Na_2SO_3 + H_2O$
$Na_2SO_3 + H_2SO_4 \to Na_2SO_4 + SO_2 + H_2O$
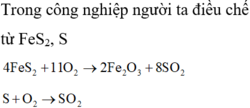
- Sự hóa than: biến hợp chất hữu cơ thành than
5)
a) \(S+O_2\underrightarrow{t^o}SO_2\)
b) \(4FeS_2+11O_2\underrightarrow{t^o}2Fe_2O_3+8SO_2\uparrow\)
c) \(2SO_2+O_2⇌2SO_3\) (điều kiện chiều thuận: to, V2O5)
d) \(nSO_3+H_2SO_4\rightarrow H_2SO_4.nSO_3\)
e) \(H_2SO_4.nSO_3+nH_2O\rightarrow\left(n+1\right)H_2SO_4\)
g) \(BaCl_2+H_2SO_4\rightarrow BaSO_4\downarrow+2HCl\)
h) \(H_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+2H_2O\)
i) \(H_2SO_4+Ba\left(NO_3\right)_2\rightarrow BaSO_4\downarrow+2HNO_3\)
k) \(Na_2SO_4+BaCl_2\rightarrow BaSO_4\downarrow+2NaCl\)
m) \(Na_2SO_4+Ba\left(NO_3\right)_2\rightarrow BaSO_4\downarrow+2NaNO_3\)
o) \(Na_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4\downarrow+2NaOH\)
Thế nào là sự hóa than bởi H2SO4 đặc?
Đó là sự oxi hóa của H2SO4 đối với các hợp chất hay chất hữu cơ để sau đó các chất sản phẩm hóa than