Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
xét 1 mol nguyên tủ Crom: có số nguyên tử Crom là 6.022. 10 23 nguyên tử và khối lượng là 52.
Thể tích của 1 mol nguyên tử Crom là:
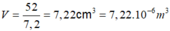
Thể tích thực của 1 nguyên tử Crom là:
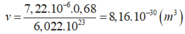
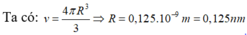

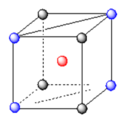
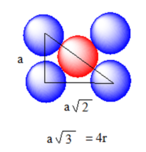
Vì M cấu tạo lập phương tâm khối nên trong 1 ô cơ sở có 2 đơn vị nguyên tử nằm vừa đủ trên đường chéo chính
Độ dài của cạnh lập phương là a → độ dài của đường chéo chính là
3
a = 4r → r =
3
.
5
,
32
.
10
-
8
4
Giả sử 1 mol nguyên tử M.
Thể tích của 1 nguyên tử M là
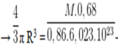
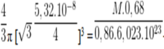
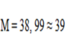
Vậy M là K.
Đáp án A.

Vì M cấu tạo lập phương tâm khối nên trong 1 ô cơ sở có 2 đơn vị nguyên tử nằm vừa đủ trên đường chéo chính
Độ dài của cạnh lập phương là a → độ dài của đường chéo chính là 3 a = 4r → r = 3 . 2 , 866 . 10 - 8 4
Giả sử 1 mol nguyên tử M.
Thể tích của 1 nguyên tử M là


Vậy M là Fe.
Đáp án B.

Đáp án A.
Trong tinh thể lập phương tâm diện, độ đặc khít là 74%.
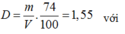
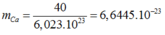
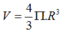
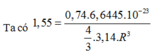
![]()

Khối lượng riêng của Cr là 7,2 g/cm3;
nghĩa là 7,2 gam Cr ↔ 7,2 ÷ 52 × 6,023 × 1023 hạt nguyên tử Cr chiếm thể tích là 1cm3 = 10-6 m3.
Lại để ý: mỗi nguyên tử chỉ chiếm 68% thể tích tinh thể (còn lại là rỗng),
nghĩa là thể tích thực của mỗi nguyên tử Crom là:
V1 nguyên tử = 10-6 × 0,68 ÷ (7,2 ÷ 52 × 6,023 × 1023)) = 4 ÷ 3πr3.
Bấm fx CASIO có ngay r = 1,25 × 10-10 m = 0,125 nm.
ta chọn đáp án B.


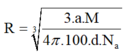 ta có:
ta có: R là Ca.
R là Ca.
Đáp án A