Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

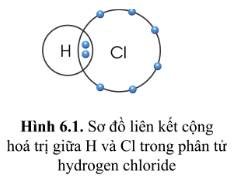
Hóa trị của H và Cl đều là I, bằng với số electron mà nguyên tử H và Cl góp chung để tạo ra liên kết.

- Nguyên tử Mg có 12 electron và 3 lớp electron
- Ion Mg2+ có 10 electron và 2 lớp electron
=> Nguyên tử Na đã mất đi 2 electron để tạo thành ion Mg2+

Ion Na+ ít hơn nguyên tử Na 1 eletron.
Ion Na+ ít hơn nguyên tử Na một lớp electron.
Hay nói cách khác nguyên tử Na cho đi 1 electron ở lớp ngoài cùng để trở thành ion mang điện tích dương, kí hiệu là Na+.

Nguyên tử Na có 1 electron ở lớp vỏ ngoài cùng (lớp 3). Ion Na+ có 8 electron ở lớp vỏ ngoài cùng (lớp 2)
Nguyên tử Cl có 7 electron ở lớp vỏ ngoài cùng (lớp 3). Ion Cl- có 8 electron ở lớp vỏ ngoài cùng (lớp 3)

a)He -> số e ngoài cùng: 2
b)Ne -> số e ngoài cùng: 8
c) Ar-> số e ngoài cùng: 8

- Số electron dùng chung của nguyên tử H và O là 4
- Trong phân tử nước:
+ Nguyên tử O có 8 electron lớp ngoài cùng => Giống khí hiếm Ne
+ Nguyên tử H có 2 electron lớp ngoài cùng => Giống khí hiếm He

a)
1 lớp:H,He
2 lớp:Li, Be, B, C, N, O, F
3 lớp:Na, Mg, Al, Si, P, S, Cl, Ar
4 lớp:K,Ca
b)
1 e ngoài cùng:H, Li, Na, K
2 e ngoài cùng:Be, Mg, Ca
3 e ngoài cùng:B, Al

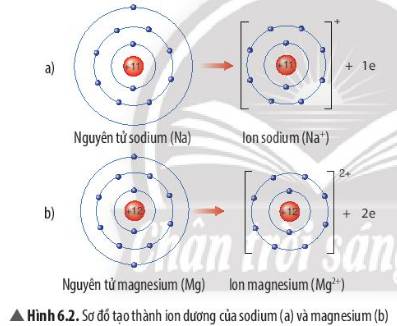
- Sự tạo thành ion sodium: Nguyên tử sodium (Na) cho đi 1 electron lớp ngoài cùng để tạo thành ion dương Na+
- Sự tạo thành ion magnesium: Nguyên tử magnesium (Mg) cho đi 2 electron lớp ngoài cùng để tạo thành ion dương Mg2+
=> Sau khi nhường electron, ion sodium và ion magnesium đều có 2 lớp electron và có 8 electron ở lớp ngoài cùng
=> Sự phân bố electron của 2 ion này giống sự phân bố electron của nguyên tử khí hiếm Neon (Ne)

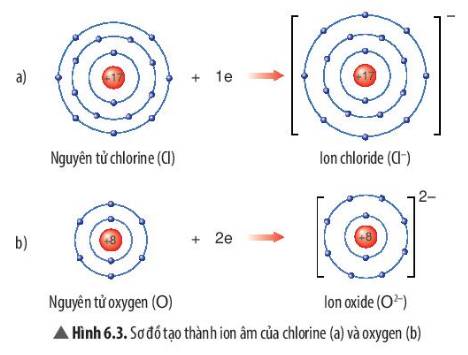
- Sự tạo thành ion chloride: Nguyên tử chlorine (Cl) nhận thêm 1 electron ở lớp ngoài cùng để tạo thành ion âm Cl-
- Sự tạo thành ion oxide: Nguyên tử oxygen (O) nhận thêm 2 electron ở lớp ngoài cùng để tạo thành ion âm O2-
- Sau khi nhận electron, ion chloride có 3 lớp electron và có 8 electron ở lớp ngoài cùng
=> Giống sự phân bố electron của nguyên tử khí hiếm Neon (Ne)
- Sau khi nhận electron, ion oxide có 2 lớp electron và có 8 electron ở lớp ngoài cùng
=> Giống sự phân bố electron của nguyên tử Argon (Ar)
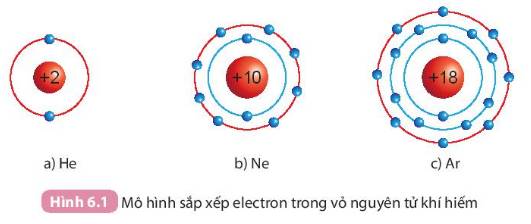




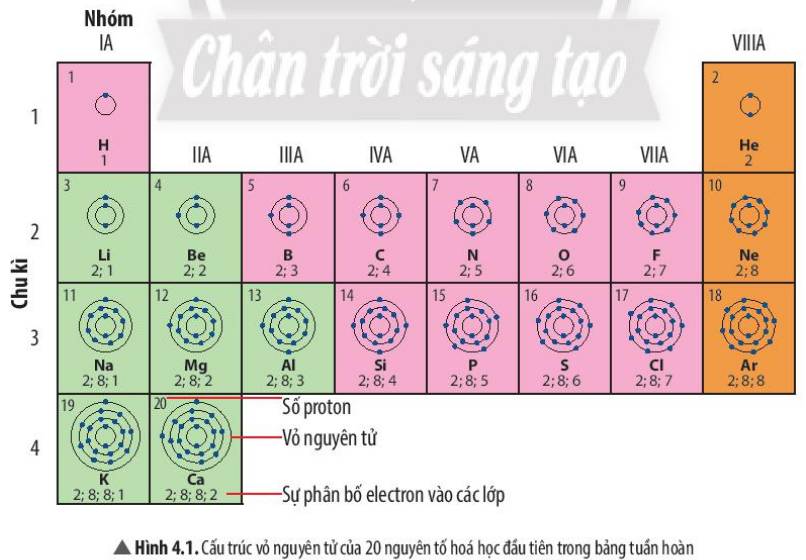
Số electron lớp ngoài cùng của Ne = Ar = 8
Số electron lớp ngoài cùng của He = 2
=>He ít số electron lớp ngoài cùng hơn Ne và Ar
Số electron lớp ngoài cùng của các nguyên tố `He` nhỏ hơn số electron ngoài cùng của nguyên tố `Ar,Ne`
Số electron ngoài cùng của nguyên tố `Ar, Ne` bằng nhau `(` đều `=8e)`