Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Từ quá trình phản ứng ta thấy số oxi hoá của các chất phản ứng ở trạng thái đầu là
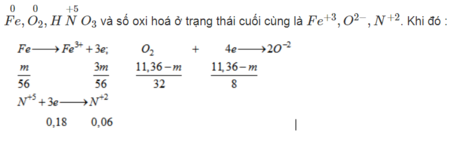
Áp dụng ĐLBT electron ta có:
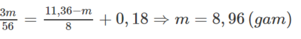

Chọn A
Cách 1:
Giả thiết hỗn hợp ban đầu được tạo ra từ a mol Fe và b mol O 2
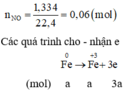

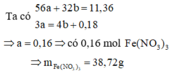
Cách 2:
Quy đổi hỗn hợp về Fe (x mol) và O (y mol)
→ 56x + 16y = 11,36 mol (1)
Bảo toàn e: 3nFe = 2nO + 3 nNO
→ 3x – 2y = 0,18 (2)
Từ (1)(2) → x = 0,16; y = 0,15
Số mol NO3- = ne cho = 3 nFe = 0,48 mol
mmuối = mFe + mNO3- = 0,16.56 + 0,48.62 = 38,72g

Coi hh gồm Fe và O.
Ta có: 56nFe + 16nO = 14,64 (1)
Ta có: \(n_{NO}=\dfrac{1,4874}{24,79}=0,06\left(mol\right)\)
Theo ĐLBT e, có: 3nFe = 2nO + 3nNO ⇒ 3nFe - 2nO = 0,06.3 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,201\left(mol\right)\\n_O=0,2115\left(mol\right)\end{matrix}\right.\)
⇒ m = mFe = 0,201.56 = 11,256 (g)

Coi hh X gồm Fe và O.
Ta có: 56nFe + 16nO = m1 (1)
\(n_{NO}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
BT e, có: 3nFe - 2nO = 3nNO = 0,06 (2)
BTNT Fe, có: nFe(NO3)3 = nFe ⇒ 242nFe = m1 + 16,68 (3)
Từ (1), (2) và (3) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,1\left(mol\right)\\n_O=0,12\left(mol\right)\\m_1=7,52\left(g\right)\end{matrix}\right.\)
BTNT N, có: nHNO3 (pư) = 3nFe(NO3)3 + nNO = 0,1.3 + 0,02 = 0,32 (mol)
⇒ nHNO3 = 0,32 + 0,32.25% = 0,4 (mol)
\(\Rightarrow m_{ddHNO_3}=\dfrac{0,4.63}{25\%}=100,8\left(g\right)\)




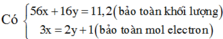
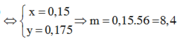


Quy đổi hh cr gồm Fe dư và các oxit sắt thành hh chỉ gồm Fe và O vs số mol lần lượt là a và b mol
mhh cr=56a+16b=11,36
KHi cho hh cr tác dụng với HNO3 loãng
nNO=0,06 mol
N+5 +3e => N+2
0,18 mol<=0,06 mol
O +2e =>O-2
b mol=>2b mol
Fe =>Fe+3 +3e
a mol =>3a mol
ne nhường=ne nhận=>0,18+2b=3a
=>a=0,16 và b=0,15
Bảo toàn Fe nFe bđ=0,16 mol=>mFe=8,96g