Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Nguyên tố R tạo thành hợp chất khí với hiđro có công thức là RH 4 sẽ tạo thành hợp chất oxit cao nhất là RO 2 có phần trăm khối lượng của nguyên tô R :
100% - 72,73% = 27,27%
72,73% phân tử khối của RO 2 ứng với 16 x 2 = 32 (đvC).
27,27% phân tử khối của RO 2 ứng với nguyên tử khối của nguyên tố R là :
32x27,27/72,73 = 12 (đvC) => R là cacbon (C)

a) CTHH oxit cao nhất là RO2
Có \(\dfrac{16.2}{M_R+16.2}.100\%=72,73\%=>M_R=12\left(g/mol\right)\)
=> R là Cacbon
b) CTHH của hợp chất R với oxi và hidro lần lượt là CO2, CH4
Ta có CTHH của h/c R với H là: RH4
<=> R mang hóa trị 4
<=> CTHH của h/c R với O là: RO2
Khối lượng mol của h/c RO2 là:
\(M_{RO_2}=\dfrac{m_O}{\%O}=\dfrac{16.2}{72,73\%}=44\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow R+16.2=44\\ \Leftrightarrow R=12\left(\dfrac{g}{mol}\right)\\ \Rightarrow R.là.C\)
b, CTHH với oxi mik có ở trên rùi và CTHH với H có trong đề bài rùi

Công thức hoá học của hợp chất có dạng XH 3 .
17,65% ứng với (3 x 1)đvC
(100 - 17,65)% ứng với 82,35x3/17,65 = 14(đvC)
Nguyên tử X có nguyên tử khối là 14, vậy nguyên tố X là nitơ (N).

Công thức hoá học các hợp chất với oxi và hiđro là CO 2 và CH 4

Gọi phi kim cần tìm là X
=> hợp chất hiđro của X là: XH 3
Ta có: phần trăm khối lượng của hiđro trong hợp chất là 17,65%
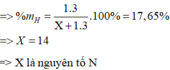
Đáp án: B
Gọi hoá trị phi kim cần tìm là n
CT với oxi : R2On ; CT với hiđrô : RH8-n
Vì n là hoá trị xét \(n\in N^{\text{*}}=\left\{1;...7\right\}\)
Ta có:
\(\frac{\left(\frac{2R}{2R+16n}\right)}{\left(\frac{R}{R+8-n}\right)}=\frac{20,25}{34}\)
\(\Rightarrow\frac{R+8-n}{R+8n}=\frac{20,25}{34}\)
Thay \(n=\left\{1;2...;7\right\}\Rightarrow n=7\Rightarrow R=80\left(Br\right)\)
b)Gọi hoá trị là x
Dùng bảo toàn khối lượng
\(\Rightarrow n_{Br2}=\frac{40,05-4,05}{80.2}=0,225\left(mol\right)\)
\(\Leftrightarrow n_M=\frac{0,225.2}{x}\Rightarrow M=\frac{4,05}{0,225.\frac{2}{x}}=9x\)
\(\Rightarrow x=3\Rightarrow M=27\left(A;\right)\)