Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

CTHH hợp chất với hidro là RH
Có \(\dfrac{M_R}{M_R+1}.100\%=97,26\%\)
=> MR = 35,5(Cl)
=> R là Cl, có số hiệu nguyên tử là 17

Để giải bài toán này, ta cần xác định nguyên tố M thuộc nhóm 4A và hợp chất khí với hiđrô gen có tỷ lệ khối lượng của nguyên tố M là 40%.
Nhóm 4A trong bảng tuần hoàn là nhóm của cacbon (C), silic (Si), germani (Ge), thiếc (Sn) và chì (Pb).
Để xác định nguyên tố M, ta cần xem xét các nguyên tố trong nhóm 4A và xem xét tỷ lệ khối lượng của chúng trong hợp chất khí với hiđrô gen.
Trong số các nguyên tố trong nhóm 4A, chỉ có cacbon (C) và silic (Si) tạo hợp chất khí với hiđrô gen.
Giả sử chúng ta có 100g hợp chất khí với hiđrô gen. Theo đề bài, tỷ lệ khối lượng của nguyên tố M là 40%, tức là 40g.
Nếu nguyên tố M là cacbon (C), thì khối lượng cacbon trong hợp chất sẽ là 40g. Tuy nhiên, cacbon không tạo hợp chất khí với hiđrô gen.
Nếu nguyên tố M là silic (Si), thì khối lượng silic trong hợp chất sẽ là 40g. Silic tạo hợp chất khí với hiđrô gen, gọi là silan (SiH4). Trong silan, tỷ lệ khối lượng của silic là 28g (khối lượng mol của silic) và tỷ lệ khối lượng của hiđrô là 4g (khối lượng mol của hiđrô). Vậy tỷ lệ khối lượng của silic là 28g / (28g + 4g) = 28% và không phải là 40%.
Vì vậy, không có nguyên tố M thuộc nhóm 4A nào trong hợp chất khí với hiđrô gen có tỷ lệ khối lượng là 40%.

a)
Nguyên tố R có cấu hình e lớp ngoài cùng là ns1
=> Công thức oxit cao nhất của R là R2O
\(\dfrac{2.M_R}{2.M_R+16}.100\%=74,19\%=>M_R=23\left(Na\right)\)
b)
TH1:
\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
______0,2----------------------->0,1
=> VH2 = 0,1.22,4 = 2,24 (l)
TH2:
\(n_{Na}=\dfrac{4,6}{23}=0,2\left(mol\right)\)
PTHH: 2Na + 2HCl --> 2NaCl + H2
_____0,2------------------------->0,1
=> VH2 = 0,1.22,4 = 2,24 (l)
c)
K --> K+ + 1e
O + 2e --> O2-
2 ion K+ và O2- trái dấu nên hút nhau bởi lực hút tĩnh điện
2K+ + O2- --> K2O

%H=100-91.176=8.824%
Gọi CTPT là RH3
R:3=91.176:8.824
=>R~31(P)
Vậy R là P

a)
R thuộc họ p và có 5 electron ở lớp ngoài cùng => R thuộc nhóm VA , trong hợp chất oxit cao nhất với oxi R có hóa trị V
=> CT : R2O5
b)
%R = \(\dfrac{2R}{2R+16.5}\).100% = 43,66% => R = 31(g/mol)
=> R là photpho (P)

Chọn B
Công thức hợp chất khí là X H 2
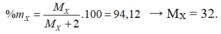
Vậy X là lưu huỳnh (S).
Công thức oxit cao nhất là S O 3
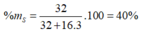


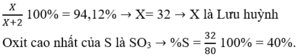
R có CH e lớp ngoài cùng ns2 np5 nên R nhóm VIIA
\(\rightarrow\) Hợp chất khí với H là HR
%H= 1,234%\(\rightarrow\)M HR= 1:1,234%= 81
\(\rightarrow\) M HR= 81-1=80.
Vậy R là brom (Br)