
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 4 :
\(n_{H2}=\dfrac{V_{H2}}{22,4}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Pt : \(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2|\)
2 3 1 3
0,1 0,15 0,05 0,15
a) \(n_{Al}=\dfrac{0,15.2}{3}=0,1\left(mol\right)\)
⇒ \(m_{Al}=n_{Al}.M_{Al}\)
= 0,1 . 27
= 2,7 (g)
\(m_{Cu}=10-2,7=7,3\left(g\right)\)
0/0Al = \(\dfrac{m_{Al}.100}{m_{hh}}=\dfrac{2,7.100}{10}=27\)0/0
0/0Cu = \(\dfrac{m_{Cu}.100}{m_{hh}}=\dfrac{7,3.100}{10}=13\)0/0
b) \(n_{Al2\left(SO4\right)3}=\dfrac{0,15.1}{3}=0,05\left(mol\right)\)
⇒ \(m_{Al2\left(SO4\right)3}=n_{Al2\left(SO4\right)3.}M_{Al2\left(SO4\right)3}\)
= 0,05 . 342
= 17,1 (g)
\(n_{H2SO4}=\dfrac{0,1.3}{2}=0,15\left(mol\right)\)
⇒ \(m_{H2SO4}=n_{H2SO4}.M_{H2SO4}\)
= 0,15 .98
= 14,7 (g)
\(C_{H2SO4}=\dfrac{m_{ct}.100}{m_{dd}}\Rightarrow m_{dd}=\dfrac{m_{ct}.100}{C}=\)\(\dfrac{14,7.100}{15}=98\left(g\right)\)
mdung dịch sau phản ứng = (mAl + mCu) + mH2SO4 - mH2
= 10 + 98 - (0,15 . 2)
=107,7 (g)
\(C_{Al2\left(SO4\right)3}=\dfrac{m_{ct}.100}{m_{dd}}=\dfrac{17,1.100}{107,7}=15,88\)0/0
Chúc bạn học tốt



a)
(1) \(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
(2) \(Fe+\dfrac{3}{2}Cl_2\xrightarrow[]{t^o}FeCl_3\)
(3) \(FeCl_2+\dfrac{1}{2}Cl_2\rightarrow FeCl_3\)
(4) \(2FeCl_3+Fe\rightarrow3FeCl_2\)
(5) \(FeCl_2+2KOH\rightarrow Fe\left(OH\right)_2+2KCl\)
(6) \(FeCl_3+3KOH\rightarrow Fe\left(OH\right)_3+3KCl\)
(7) \(Fe\left(OH\right)_2\xrightarrow[không.có.Oxi]{t^o}FeO+H_2O\)
(8) \(2Fe\left(OH\right)_3\xrightarrow[]{t^o}Fe_2O_3+3H_2O\)
(9) \(4Fe\left(OH\right)_2+O_2+2H_2O\rightarrow4Fe\left(OH\right)_3\)
(10) \(2FeO+\dfrac{1}{2}O_2\xrightarrow[]{t^o}Fe_2O_3\)
(11) \(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
(12) \(Fe_2O_3+3CO\xrightarrow[]{t^o}2Fe+3CO_2\)
(13) \(2FeO+4H_2SO_{4\left(đ\right)}\xrightarrow[]{t^o}Fe_2\left(SO_4\right)_3+SO_2+4H_2O\)
(14) \(FeO+CO\xrightarrow[]{t^o}Fe+CO_2\)
c)
\(Ca+2H_2O\rightarrow Ca\left(OH\right)_2+H_2\uparrow\)
\(Ca\left(OH\right)_2+2HCl\rightarrow CaCl_2+2H_2O\)
\(CaCl_2+K_2CO_3\rightarrow2KCl+CaCO_3\)
\(CaCO_3+CO_2+H_2O\rightarrow Ca\left(HCO_3\right)_2\)
\(Ca\left(HCO_3\right)_2+2KOH\rightarrow CaCO_3+K_2CO_3+2H_2O\)
\(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\)

Câu 4 :
\(n_{Fe2O3}=\dfrac{24}{160}=0,15\left(mol\right)\)
Pt : \(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O|\)
1 3 1 3
0,15 0,15
a) \(n_{Fe2\left(SO4\right)3}=\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
⇒ \(m_{Fe2\left(SO4\right)3}=0,15.400=60\left(g\right)\)
b) \(C_{M_{Fe2\left(SO4\right)3}}=\dfrac{0,15}{0,5}=0,3\left(M\right)\)
Chúc bạn học tốt
a,\(n_{Fe_2O_3}=\dfrac{24}{160}=0,15\left(mol\right)\)
PTHH: Fe2O3 + 3H2SO4 → Fe2(SO4)3 + 3H2O
Mol: 0,15 0,45 0,15
\(m_{Fe_2\left(SO_4\right)_3}=0,15.400=60\left(g\right)\)
b,\(C_{M_{ddFe_2\left(SO_4\right)_3}}=\dfrac{0,15}{0,5}=0,3\left(mol\right)\)

- NaHCO3: Tạo ra khí CO2 tan ít trong nước--> Thỏa mãn
\(2NaHCO_3\underrightarrow{t^o}Na_2CO_3+CO_2+H_2O\)
- NH4Cl và CaO: Tạo ra khí NH3, HCl tan nhiều trong nước --> không thỏa mãn
\(NH_4Cl\underrightarrow{t^o}NH_3+HCl\)
- CH3COONa, NaOH, CaO: Tạo khí CH4 tan ít trong nước --> Thỏa mãn
\(CH_3COONa+NaOH\underrightarrow{t^o,CaO}CH_4+Na_2CO_3\)
- KMnO4: Tạo khí O2 tan ít trong nước --> Thỏa mãn
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)

PTHH: Al2O3+6HCl➝2AlCl3+3H2O(1)
a)nAl2O3=\(\dfrac{10,2}{102}\)=0,1(mol)
mHCl=\(\dfrac{5\%.219}{100\%}\)=10,95(g)
⇒nHCl=\(\dfrac{10,95}{36,5}\)=0,3(mol)
Xét tỉ lệ Al2O3:\(\dfrac{0,1}{1}\)=0,1
Xét tỉ lệ HCl:\(\dfrac{0,3}{6}\)=0,05
⇒HCl pứng hết,Al2O3 còn dư
Theo PTHH(1) ta có nAl2O3 pứng=\(\dfrac{nHCl}{6}\)=\(\dfrac{0,3}{6}\)=0,05(mol)
⇒nAl2O3 dư=nAl2O3ban đầu-nAl2O3 pứng=0,1-0,05=0,05(mol)
⇒mAl2O3 dư=0,05.102=5,1(g)
b) C%HCl=\(\dfrac{0,3.36,5}{219+10,2}\).100%=4,8%
nAlCl3=0,1(mol)
⇒C%AlCl3=\(\dfrac{0,1.136,5}{10,2+219}\).100%=6%



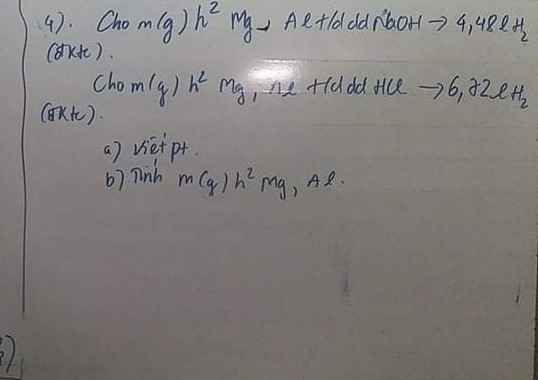



 giúp mình với ạ , mình đang cần gấp ạ, các bạn làm theo cách kẻ bảng ra giúp mình được không ạ
giúp mình với ạ , mình đang cần gấp ạ, các bạn làm theo cách kẻ bảng ra giúp mình được không ạ Mk đang cần gấp, mn giúp mình vs ạ
Mk đang cần gấp, mn giúp mình vs ạ
Bài 2 :
Pt : \(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
0,2 0,2 0,2
a) \(m_{CuO}=25,6-9,6=16\left(g\right)\)
b) Có : \(m_{CuO}=16\left(g\right)\)
\(n_{CuO}=\dfrac{16}{80}=0,2\left(mol\right)\)
\(n_{CuSO4}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{CuSO4}=0,2.160=32\left(g\right)\)
c) \(n_{H2SO4}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{H2SO4}=0,2.98=19,6\left(g\right)\)
\(C_{ddH2SO4}=\dfrac{19,6.100}{150}\simeq13,07\)0/0
Chúc bạn học tốt