Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a,2KMnO_4\rightarrow\left(t^o\right)K_2MnO_2+MnO_2+O_2\\ b,n_{KMnO_4}=\dfrac{31,6}{158}=0,2\left(mol\right)\\ \Rightarrow n_{O_2}=\dfrac{0,2}{2}=0,1\left(mol\right)\\ \Rightarrow V_{O_2\left(đktc\right)}=0,1.22,4=2,24\left(l\right)\\ c,n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\\ 3Fe+2O_2\rightarrow\left(t^o\right)Fe_3O_4\\ Vì:\dfrac{0,2}{3}< \dfrac{0,1}{2}\Rightarrow Fedư\\ \Rightarrow n_{Fe_3O_4}=n_{O_2}:2=0,1 :2=0,05\left(mol\right)\\ \Rightarrow m_{Fe_3O_4}=232.0,05=11,6\left(g\right)\)

Sửa "nguyên tử nguyên tố" thành "nguyên tử" thôi nhé! Sao dạo này ai cũng lạm dụng từ trên trong khi nó chả đúng tí nào hết nhỉ?Mà mình ko chắc câu b đâu.
a)Theo đề bài: \(X+4.1=16\)(đvC) (vì 1 nguyên tử X + 4 nguyên tử Hiđro = nguyên tử Oxi)
Do đó \(x=16-4=12\)
Vậy X là Cacbon (KHHH: C)
b)Từ câu a suy ra công thức hóa học của hợp chất trên là: CH4
\(\%C=\frac{M_C}{M_{CH_4}}.100=\frac{12}{16}.100=75\%\)
Vậy C nặng 75 % trên tổng khối lượng của hợp chất.
\(\Rightarrow\)4 nguyên tử H nặng 25% khối lượng của hợp chất.
a/ Gọi công thức có dạng là XH4
Vì 1 nguyên tử X liên kết với 4 nguyên tử H nặng bằng nguyên tử Oxi nên ta có X+4=16
=> X=12
=> nguyên tố X là C(cacbon)
=> CTHH là CH4
b, Ta có:
%C(CH4) = M(C)/M(C+4.H).100%
= 12/(12+4).100
= 75%

a. \(d_{\dfrac{A}{kk}=2}\Rightarrow2.29=58\left(\dfrac{g}{mol}\right)\)
\(m_C=\dfrac{58.82,76\%}{100\%}=48\left(g\right)\\ n_C=\dfrac{48}{12}=4\left(mol\right)\)
\(m_H=\dfrac{58.17,24\%}{100\%}=10\left(g\right)\)
\(n_H=\dfrac{10}{1}=10\left(mol\right)\)
CTHH : C4H10
b. \(n_{C_4H_9}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\\ m_{C_4H_9}=0,05.58=2,9\left(g\right)\)

a) mBr = 1.80 = 80 (g)
b) mC6H12O6 = 1.180=180(g)
c) mFe3O4 = 1.232= 2332(g)
\(a.m_{Br}=1.80=80\left(g\right)\\ b.m_{C_6H_{12}O_6}=1.180=180\left(g\right)\\ c.m_{Fe_3O_4}=\dfrac{N}{6.10^{23}}.232\left(g\right)\)

Natri (Na):

Nhôm (Al):

Thủy ngân (Hg):

Cacbon monoxit (CO):

Natri hidroxit (NaOH):

Metan (CH4):
Đồng monoxit (CuO)




a) \(m_{CuSO_4}=0,3.160=48\left(g\right)\)
b) \(n_{CaCO_3}=\dfrac{9.10^{23}}{6.10^{23}}=1,5\left(mol\right)=>m_{CaCO_3}=1,5.100=150\left(g\right)\)
c) \(n_{MgCl_2}=\dfrac{1,5.10^{22}}{6.10^{23}}=0,025\left(mol\right)=>m_{MgCl_2}=0,025.95=2,375\left(g\right)\)
e) \(n_{CO_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)=>m_{CO_2}=0,1.44=4,4\left(g\right)\)
f) \(n_{NaOH}=\dfrac{0,25.10^{24}}{6.10^{23}}=\dfrac{5}{12}\left(mol\right)=>m_{NaOH}=\dfrac{5}{12}.40=16,667\left(g\right)\)

Câu 1:
- Hóa trị của N trong HNO3 là IV
Do không có phân lớp d trống, nên N chỉ có hoá trị TỐI ĐA là 4 (3 góp chung e + 1 cho nhận).
- Hóa trị của N trong NxOy là y
- Hóa trị của N trong NO2 là IV

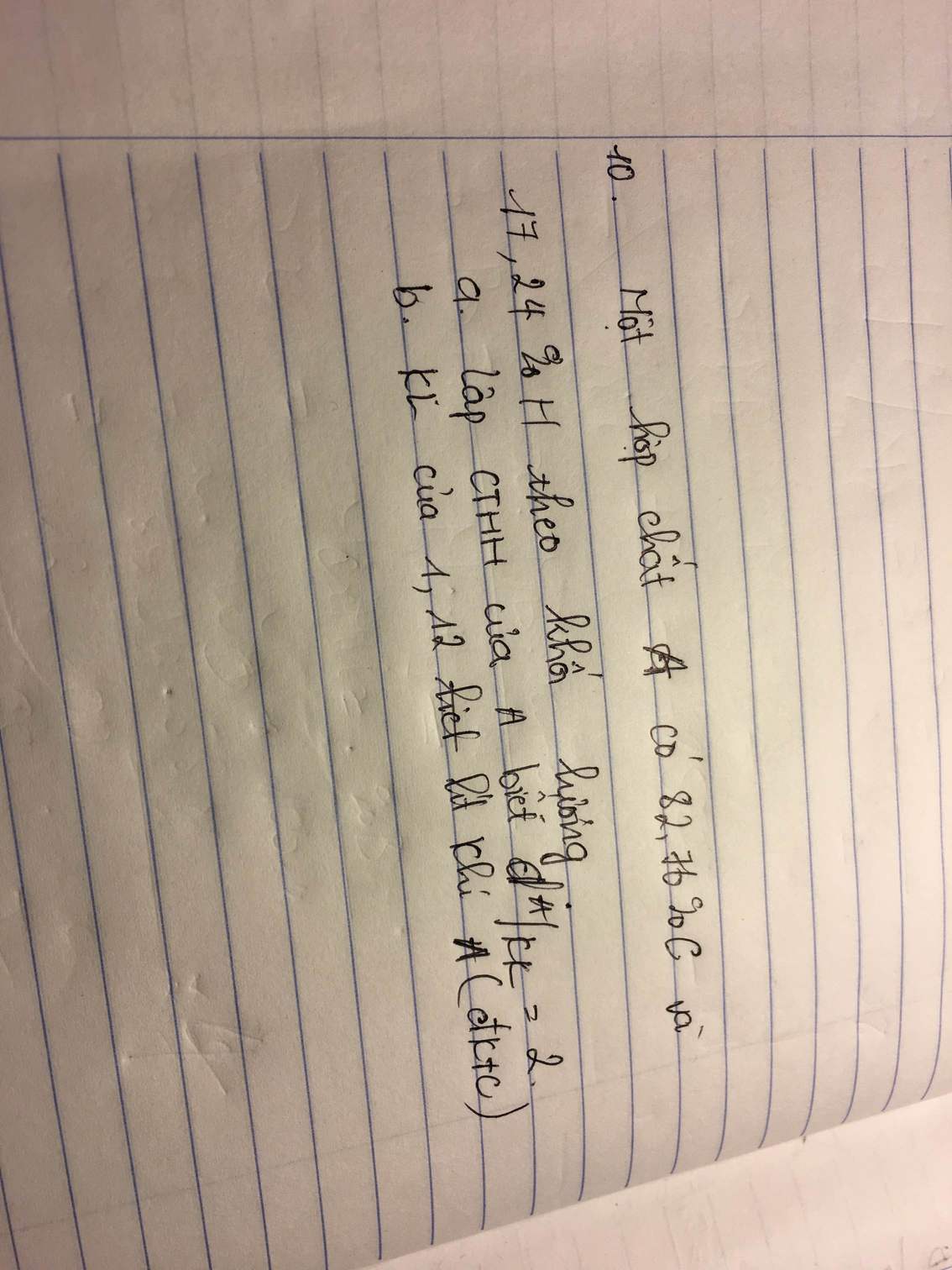

a,\(m_{CuSO_4}=0,25.160=40\left(g\right)\)
b, \(n_{NaCl}=\dfrac{1,5.10^{23}}{6.10^{23}}=0,25\left(mol\right)\)
\(m_{NaCl}=0,25.58,5=14,625\left(g\right)\)
\(m=n.M=0,25.160=40\left(g\right)\)
\(n_{NaCl}=\dfrac{1,5.10^{23}}{6.10^{23}}=0,25\left(mol\right)\\ m=n.M=0,25.58,5=14,625\left(g\right)\)