
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Bài 6 :
$a) H_2SO_4 + BaCl_2 \to BaSO_4 + 2HCl$
$b) CaCO_3 + 2HNO_3 \to Ca(NO_3)_2 + CO_2 + H_2O$
$c) 2KOH + 2NaHSO_4 \to Na_2SO_4 + K_2SO_4 + 2H_2O$
$d) CuO + 2HCl \to CuCl_2 + H_2O$
$e) SO_2 + NaOH \to NaHSO_3$
$g) CO_2 + 2NaOH \to Na_2CO_3 + H_2O$
Câu 7 :
CTHH lần lượt là : $HBr,H_2SiO_3,HMnO_4,H_2Cr_2O_7$



Cho nước vào các hóa chất dạng bột
+ Tan : Na2O, NaCl
\(Na_2O+H_2O\rightarrow2NaOH\)
+ Tan, có vẩn đục : CaO
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
+ Không tan: Al2O3, Fe2O3, MgO
Cho quỳ tím vào 2 dung dịch tan
+ Quỳ hóa xanh: Na2O
+ Không đổi màu : NaCl
Cho từ từ đến dư dung dịch của lọ Na2O vào các mẫu thử không tan
+ Tan : \(Al_2O_3+2NaOH\rightarrow2NaAlO_2+H_2O\)
+ Không tan :Fe2O3, MgO
Quan sát màu sắc của 2 chất rắn không tan
+ Chất bột có màu nâu đỏ là Fe2O3
+ Chất bột có màu trắng là MgO

Câu 40. \(n_{NaOH}=\dfrac{20}{40}=0,5\left(mol\right);n_{HCl}=\dfrac{36,5}{36,5}=1\left(mol\right)\)
PTHH: \(NaOH+HCl\rightarrow NaCl+H_2O\)
Theo đề: 0,5mol .....1mol
Lập tỉ lệ : \(\dfrac{0,5}{1}< \dfrac{1}{1}\)=> Sau phản ứng NaOH hết, HCl dư
=> Thử môi trường sau phản ứng bằng quỳ sẽ có màu đỏ
Câu 41.
nNaOH=0,3.0,5=0,15(mol);nHCl=0,3.1=0,3(mol)
PTHH: NaOH + HCl → NaCl + H2O
Theo đề:0,15mol ....0,3mol
Lập tỉ lệ :\(\dfrac{0,15}{1}< \dfrac{0,3}{1}\)=> Sau phản ứng NaOH hết, HCl dư
=> Dung dịch sau phản ứng làm quỳ tím hóa màu đỏ

Câu 25: (NH4)2HPO4 chứa N (đạm) và P (lân)
=> Chọn B
Câu 26: Chọn A
Tạo kết tủa xanh lơ là Cu(NO3)2
Cu(NO3)2 + 2NaOH ---> Cu(OH)2 + 2NaNO3
Tạo kết tủa nâu đỏ là Fe(NO3)3
Fe(NO3)3 + 3NaOH ---> Fe(OH)3 + 3NaNO3
Không hiện tượng là KNO3
Câu 27: \(n_{CO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
PTHH: Na2CO3 + 2HCl ---> 2NaCl + CO2 + H2O
0,15<----------------------------0,15
=> \(a=m_{Na_2CO_3}=0,15.106=15,9\left(g\right)\)
=> Chọn A
Câu 28: Chọn C (Fe bị thụ động trong H2SO4 đặc, nguội)

- Trích mẫu thử.
- Cho quỳ tím vào các mẫu thử:
+ Quỳ tím hóa đỏ: HCl, H2SO4(1)
+ Quỳ tím ko đổi màu: NaNO3
- Cho BaCl2 vào nhóm (1)
+ Xuất hiện kết tủa: H2SO4
+ Ko kết tủa: HCl
PTHH: \(BaCl_2+H_2SO_4\rightarrow2HCl+BaSO_4\downarrow\)

Bài 8:
Đặt CTTQ oxit kim loại hóa trị III là A2O3 (A là kim loại)
nH2SO4=0,3(mol)
mNaOH=24%. 50= 12(g) => nNaOH=0,3(mol)
PTHH: 2 NaOH + H2SO4 -> Na2SO4 + 2 H2O
0,3________0,15(mol)
A2O3 +3 H2SO4 -> A2(SO4)3 +3 H2
0,05___0,15(mol)
=> M(A2O3)= 8/0,05=160(g/mol)
Mặt khác: M(A2O3)=2.M(A)+ 48(g/mol)
=>2.M(A)+48=160
<=>M(A)=56(g/mol)
-> Oxit cần tìm: Fe2O3
Bài 7:
mHCl= 547,5. 6%=32,85(g) => nHCl=0,9(mol)
Đặt: nZnO=a(mol); nFe2O3=b(mol) (a,b>0)
PTHH: ZnO +2 HCl -> ZnCl2+ H2O
a________2a_______a(mol)
Fe2O3 + 6 HCl -> 2 FeCl3 + 3 H2O
b_____6b____2b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}81a+160b=28,15\\2a+6b=0,9\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,15\\b=0,1\end{matrix}\right.\)
=> mFe2O3=0,1.160=16(g)
=>%mFe2O3=(16/28,15).100=56,838%
=>%mZnO= 43,162%
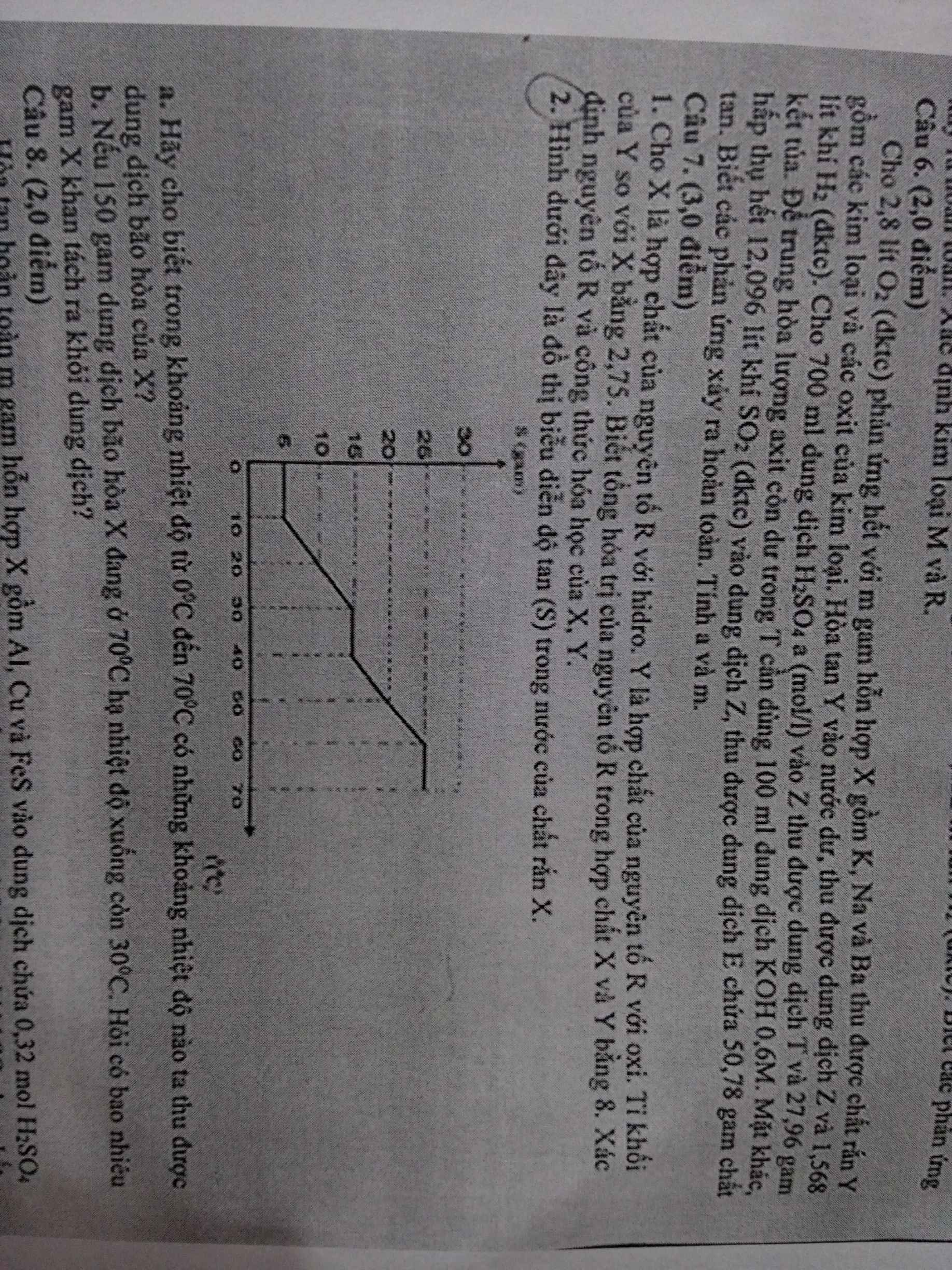












a) Những khoảng nhiệt độ mà dd X bão hòa:
+ 0-10oC
+ 30-40oC
+ 60-70oC
b)
- Xét khoảng 60-70oC:
Gọi khối lượng NaCl trong dd bão hòa tại khoảng nhiệt độ này là a (g)
\(S_{70^oC}=\dfrac{a}{150-a}.100=25\left(g\right)\)
=> a = 30 (g)
=> \(m_{H_2O}=150-30=120\left(g\right)\)
- Xét khoảng 30-40oC:
Gọi khối lượng NaCl trong dd bão hòa tại nhiệt độ này là b (g)
\(S_{30^oC}=\dfrac{b}{120}.100=15\)
=> b = 18 (g)
=> mNaCl(tách ra) = 30 - 18 = 12 (g)
ý 2 đúng không :)