Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đồ thị trải qua các giai đoạn:
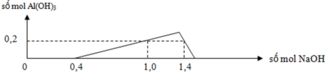
+Giai đoạn chưa xuất hiện kết tủa do NaOH tác dụng với H2SO4.
+Kết tủa tăng dần đến cực đại do NaOH tác dụng với Al2(SO4)3tạo kết tủa Al(OH)3.
+Kết tủa giảm dần do NaOH hòa tan Al(OH)3.
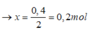
Nhận thấy lúc 1 mol NaOH phản ứng và 1,4 mol NaOH phản ứng đều thu được cùng một lượng kết tủa, chứng tỏ 0,4 mol NaOH chênh lệch đã tạo 1 lượng kết tủa và hòa tan lượng kết tủa đó.
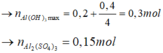
Cho 0,7 mol Ba(OH)2 vào X thì kết tủa thu được gồm BaSO40,65 mol và Al(OH)3.
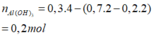
Vậy m=167,05 gam

Đáp án : B
+) Tại nNaOH = 0,4 mol thì trung hòa vừa hết axit
=> x = 0,2 mol
Tại nNaOH = 1 mol => Al3+ dư
Tại nNaOH = 1,4 mol thì kết tủa tan 1 phần
n A l ( O H ) 3 = 4 n A l 3 + - n N a O H - n H C l
⇒ n A l 3 + = 0 , 3 m o l
=> y = 0,15 mol
Nếu thêm n B a O H 2 = 0 , 05 m o l vào X :
=> Kết tủa : 0,2 mol Al(OH)3 và 0,5 mol BaSO4
=> m = 132,1g

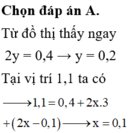
| CHÚ Ý |
| + Với các loại bài toán về đồ thị để giải nhanh và chính xác được các bạn nên tư duy theo hướng phân chia nhiệm vụ của yếu tố thuộc trục hoành. + Với bài toán này ở mỗi giai đoạn Ba(OH2) làm những nhiệm vụ sau: Giai đoạn 1: Trung hòa H+ Giai đoạn 2: Đưa kết tủa lên cực đại. Giai đoạn 3: Hòa tan kết tủa Al(OH)3 |

Đáp án A
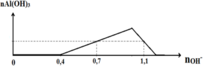
Từ đồ thị thấy ngay 2y = 0,4 → y = 0,2
Tại vị trí 1,1 ta có: 1,1= 0,4+2x.3+(2x-0,1)=> x= 0,1

Đáp án B
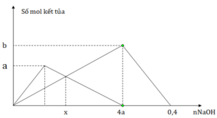
Dựa vào đồ thị thấy tại 6,99 gam thì lượng kết tủa không đổi → tại đó chỉ có kết tủa BaSO4: 0,03 mol → a = (0,03 : 3): 0,1 = 0,1
Nếu cho (Ba(OH)2 0,02 mol và NaOH 0,03 mol) + Al2(SO4)3: 0,01mol
Thấy 3< n O H - : n A l 3 + < 4 → Tạo đồng thời Al(OH)3: x mol và AlO2-: y mol
Ta có hệ phương trình
x + y = 0 , 02 3 x + 4 y = 0 , 07 → x = 0,01; y = 0,01
Mặt khác: n S O 4 2 - = 0,03 mol > n B a 2 + = 0,02 mol → BaSO4 ; 0,02 mol
→ m k t = m A l ( O H ) 3 + m B a S O 4 = 0,01*78 + 0,02*233 = 5,44 gam

Chọn đáp án B
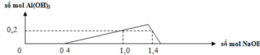
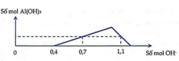
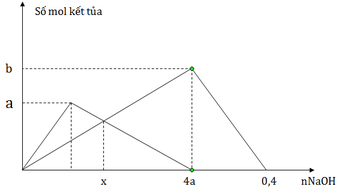
Nhìn đồ thị ta thấy có 3 giai đoạn
+ giai đoạn 1: đồ thị đi lên khi xảy ra phản ứng:
3Ba(OH)2 + Al2(SO4)3→ 3BaSO4↓ + 2Al(OH)3↓ (1)
+ giai đoạn đồ thị đi xuống là do Ba(OH)2 đang hòa tan kết tủa Al(OH)3↓ theo phản ứng
Ba(OH)2 + 2Al(OH)3→ Ba(AlO2)2 + 4H2O (2)
+ giai đoạn đồ thị đi ngang khi phản ứng (2) Al(OH)3 bị hòa tan hoàn toàn, chỉ còn lại kết tủa BaSO4
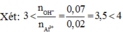
nBa(OH)2 = 0,1. 0,2 = 0,02 (mol) ; nNaOH = 0,1.0,3 = 0,03 (mol) ; nAl2(SO4)3 = 0,1.0,1 = 0,01 (mol)
=> ∑ nOH- = 2nBa(OH)2 + nNaOH = 2. 0,02 + 0,03 = 0,07 (mol)
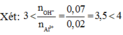
Có các phản ứng xảy ra:
Ba2+ + SO42-→ BaSO4↓
0,02 → 0,02 (mol)
3OH- + Al3+ → Al(OH)3↓
4OH- + Al3+ → AlO2− + H2O
Áp dụng công thức nhanh:
nOH- = 4nAl3+ - nAl(OH)3
=> nAl(OH)3 = 4nAl3+ - nOH- = 4.0,02 – 0,07 = 0,01 (mol)
=> m↓ = mAl(OH)3 + mBaSO4 = 0,01.78 + 0,02.233 = 5,44 (g) gần nhất với 5,45 (g)




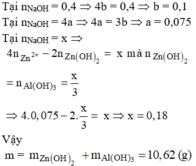
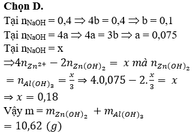
Đáp án C
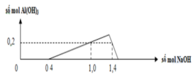
Đồ thị trải qua các giai đoạn:
+Giai đoạn chưa xuất hiện kết tủa do NaOH tác dụng với H2SO4.
+Kết tủa tăng dần đến cực đại do NaOH tác dụng với Al2(SO4)3tạo kết tủa Al(OH)3.
+Kết tủa giảm dần do NaOH hòa tan Al(OH)3.
Nhận thấy lúc 1 mol NaOH phản ứng và 1,4 mol NaOH phản ứng đều thu được cùng một lượng kết tủa, chứng tỏ 0,4 mol NaOH chênh lệch đã tạo 1 lượng kết tủa và hòa tan lượng kết tủa đó.
Cho 0,7 mol Ba(OH)2 vào X thì kết tủa thu được gồm BaSO40,65 mol và Al(OH)3.
Vậy m=167,05 gam