Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Áp dụng định luật bảo toàn khối lượng ta có:
mđầu = msau ⇒ nđầu.Mđầu = nsau.Msau
→ n s a u n đ ầ u = M đ ầ u M s a u h a y n 2 n 1 = M 2 M 1
Ta có công thức rất quan trọng là
n đ ầ u - n s a u = n 1 - n 2 = n H 2 p h ả n ứ n g - n π phản ứng
Vậy mục tiêu của ta bây giờ là đi tính n2.
Ta lần lượt có n1 = 0,1 + 0,2 + 0,3 = 0,6 mol.
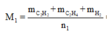
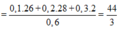
Mà M2 = 11. M H 2 = 11.2 = 22 nên từ:
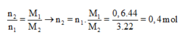
![]()
Phải hiểu rằng n2 = 0,2 mol nghĩa là số mol H2 đã phản ứng là 0,2 mol hay cũng chính là số mol π đã phản ứng là 0,2.
Do đó để tính a là số mol tối đa hỗn hợp Y phản ứng với Br2 trong dung dịch thì ta chỉ cần lấy số mol π ban đầu trừ đi số mol π ban đầu đã phản ứng, hay ta có
a = nπ (đầu) – nπ (đã phản ứng) = 0,1.2 + 0,2.1 –(0,6 – 0,4) = 0,2 mol
Đáp án B

Đáp án C
Hỗn hợp T là hai axit cacboxylic đơn chức → R1COOH,R2COOH
Z là este được tạo bởi T và etylen glicol → este 2 chức → R1OOC−CH2−CH2−COOR2
- Quá trình 1:
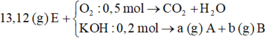
Gọi a, b, c lần lượt là mol của 2 axit trong T, Z.
+ Ta có:
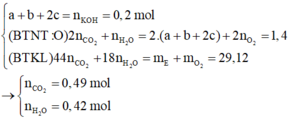
- Quá trình 2: Khi cho E tác dụng với dung dịch Br2, nhận thấy ![]()
Trong A chỉ có 1 chất tham gia phản ứng cộng Br2 khi đó Z được tạo bởi A cũng có phản ứng cộng Br2.
+ Gọi X là axit có 2 liên kết: a mol
+ Gọi Y là axit có chứa 1 liên kết: b mol
→ Z là este của axit X, Y → có chứa 3 liên kết: c mol
+ Ta có hệ sau:
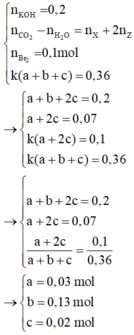
Bảo toàn C: n.0,03 + m.0,13 + 0,02. (n+m+2) =0,49
(với n,m là số C của X, Y với n ≥ 3 và m ≥ 2).
+ Xét n = 3 suy ra n = 2. Từ đó Z gồm
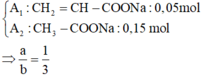
+ Nếu n > 3 thì m < 2: không thỏa mãn
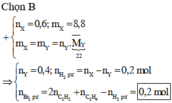
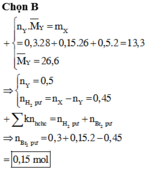


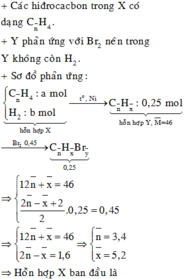
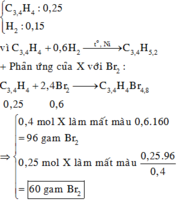
Đáp án A