Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Định hướng tư duy giải
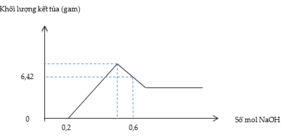
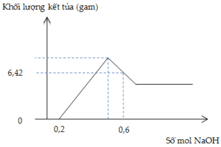
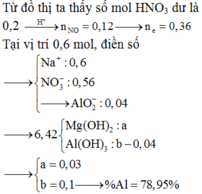
Từ đồ thị ta thấy số mol HNO3 dư là 0,2 → H + n N O = 0 , 12 → n e = 0 , 36
Tại vị trí 0,6 mol, điền số
→ N a + : 0 , 6 N O 3 - : 0 , 56 → A l O 2 - : 0 , 04 → 6 , 42 M g ( O H ) 2 : a A l ( O H ) 3 : b - 0 , 04 → a = 0 , 03 b = 0 , 1 → % A l = 78 , 95 %

Chọn đáp án C
Định hướng tư duy giải
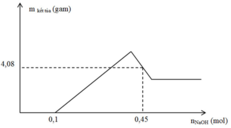
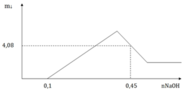
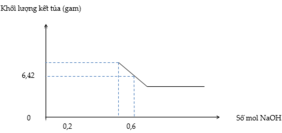
Từ đồ thị ta thấy số mol HNO3 dư là 0,1 → H + n N O = 0 , 1 → n e = 0 , 3
Tại vị trí 0,45 mol
→ D S N a + : 0 , 45 N O 3 - : 0 , 4 → A l O 2 - : 0 , 05 → m A l + M g + 0 , 3 . 17 - 0 , 05 . 78 = 4 , 08 → m A l + M g = 2 , 88 → m m u ố i = 2 , 88 + 0 , 3 . 62 = 21 , 48

Chọn C.
- Các phương trình phản ứng:
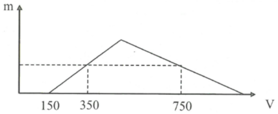
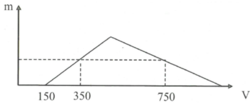
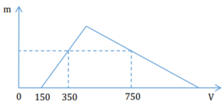
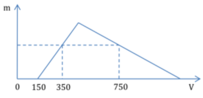
+ Đoạn từ 0 đến 150 (trung hòa NaOH dư): H + + O H - → H 2 O
Với: nH+ = nNaOH (dư) = 0,15 mol.
+ Đoạn từ 150 đến 350 (tạo kết tủa): A l 3 + + 3 O H - → A l ( O H ) 3
Với: n A l O 2 - = n H + = n A l ( O H ) 3 = 0 , 35 - 0 , 15 = 0 , 2 m o l .
+ Đoạn từ 350 đến 750 (kết tủa tan vào dung dịch): A l 3 + + 3 O H - → A l ( O H ) 3 .
Với: n A l O 2 - = n H + 4 = 0 , 75 - 0 , 35 4 = 0 , 1 m o l
- Tổng số n A l O 2 - đã dùng: ∑ n A l O 2 - = n N a A l O 2 = 0 , 2 + 0 , 1 = 0 , 3 m o l
- Áp dụng các định luật bảo toàn nguyên tố cho Al và Na, ta được:
n A l 2 O 3 = n A l O 2 - 2 = 0 , 3 2 = 0 , 15 m o l
Và n N a 2 O = n N a O H + n N a A l O 2 2 = 0 , 15 + 0 , 3 2 = 0 , 255 m o l
- Khối lượng hỗn hợp Al2O3 và Na2O: a = 0,15.102 + 0,225.62 = 29,25 gam.
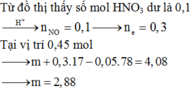







Đáp án C
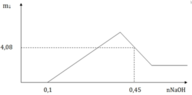
Khi nOH- = 0,1 mol thì kết tủa mới xuất hiện nên nH+ dư = 0,1 mol → nH+ pứ = 0,4 mol
→ nNO = 0,1 mol
Đặt a, b là số mol Al và Mg
Áp dụng bảo toàn electron ta có: 3.nAl + 2.nMg = 3.nNO suy ra 3a + 2b = 3.0,1 (1)
Khi nOH- = 0,45 mol thì kết tủa thu được gồm Mg(OH)2 b mol; Al(OH)3 (4,08-58b)/78 mol
Suy ra 0,45 = 0,1 + 2b + 4a - (4,08-58b)/78 (2)
Giải hệ (1) và (2) ta có a = 0,08 và b = 0,03
Suy ra m = 2,88 gam