Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

PT: \(Mg+H_2SO_4\rightarrow MgSO_4+H_2\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
a, Giả sử: \(\left\{{}\begin{matrix}n_{Mg}=x\left(mol\right)\\n_{Al}=y\left(mol\right)\end{matrix}\right.\)
⇒ 24x + 27y = 12,6 (1)
Ta có: \(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
Theo PT: \(n_{H_2}=n_{Mg}+\dfrac{3}{2}n_{Al}=x+\dfrac{3}{2}y\left(mol\right)\)
\(\Rightarrow x+\dfrac{3}{2}y=0,6\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,3\left(mol\right)\\y=0,2\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{MG}=\dfrac{0,3.24}{12,6}.100\%\approx57,1\%\\\%m_{Al}\approx42,9\%\end{matrix}\right.\)
b, Theo PT: \(\left\{{}\begin{matrix}n_{H_2SO_4}=n_{H_2}=0,6\left(mol\right)\\n_{MgSO_4}=n_{Mg}=0,3\left(mol\right)\\n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Al}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{H_2SO_4}=0,6.98=58,8\left(g\right)\Rightarrow m_{ddH_2SO_4}=\dfrac{58,8}{14,7\%}=400\left(g\right)\)
Ta có: m dd sau pư = 12,6 + 400 - 0,6.2 = 411,4 (g)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{MgSO_4}=\dfrac{0,3.120}{411,4}.100\%\approx8,75\%\\C\%_{Al_2\left(SO_4\right)_3}=\dfrac{0,1.342}{411,4}.100\%\approx8,31\%\end{matrix}\right.\)
Bạn tham khảo nhé!

\(n_{H_2}=\dfrac{8,96}{22,4}=0,4(mol)\\ n_{Al}=x(mol);n_{Mg}=y(mol)\\ \Rightarrow 27x+24y=7,8(1)\\ a,2Al+6HCl\to 2AlCl_3+3H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow 1,5x+y=0,4(2)\\ (1)(2)\Rightarrow x=0,2(mol);y=0,1(mol)\\ \Rightarrow \%_{Al}=\dfrac{0,2.27}{7,8}.100\%=69,23\%\\ \Rightarrow \%_{Mg}=100\%-69,23\%=30,77\%\)
\(b,\Sigma n_{HCl}=3x+2y=0,8(mol)\\ \Rightarrow C\%_{HCl}=\dfrac{0,8.36,5}{192,2}.100\%=15,19\%\\ c,n_{AlCl_3}=0,2(mol);n_{MgCl_2}=0,1(mol)\\ \Rightarrow C\%_{AlCl_3}=\dfrac{0,2.133,5}{0,2.27+192,2-0,3.2}.100\%=13,55\%\\ C\%_{MgCl_2}=\dfrac{0,1.95}{0,1.24+192,2-0,1.2}.100\%=4,89\%\)

a) \(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
______0,2---->0,3------------>0,1------>0,3______(mol)
=> VH2 = 0,3.22,4= 6,72(l)
b) \(C_{M\left(H_2SO_4\right)}=\dfrac{0,3}{0,1}=3M\)
\(C_{M\left(Al_2\left(SO_4\right)_3\right)}=\dfrac{0,1}{0,1}=1M\)
Câu 3:
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ PTHH:Mg+2HCl\to MgCl_2+H_2\\ MgO+2HCl\to MgCl_2+H_2O\\ \Rightarrow n_{Mg}=n_{H_2}=0,3(mol)\\ \Rightarrow \%_{Mg}=\dfrac{0,3.24}{15,2}.100\%=47,37\%\\ \Rightarrow \%_{MgO}=100\%-47,37\%=52,63\%\)
\(n_{MgO}=\dfrac{15,2-0,3.24}{40}=0,2(mol)\\ \Rightarrow \Sigma n_{HCl}=0,3.2+0,2.2=1(mol)\\ \Rightarrow m_{dd_{HCl}}=\dfrac{1.36,5}{10\%}=365(g)\\ \Sigma n_{MgCl_2}=0,2+0,3=0,5(mol)\\ \Rightarrow C\%_{MgCl_2}=\dfrac{0,5.95}{15,2+365}.100\%=12,49\%\)
\(PTHH:Mg+2H_2SO_{4(đ)}\to MgSO_4+2H_2O+SO_2\uparrow\\ MgO+H_2SO_4\to MgSO_4+H_2O\\ \Rightarrow n_{SO_2}=n_{Mg}=0,3(mol)\\ \Rightarrow V_{SO_2}=0,3.22,4=6,72(l)\)

2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
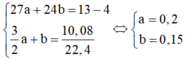
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.

\(n_{H_2}=\dfrac{4,368}{22,4}=0,195mol\)
\(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\Rightarrow27x+24y=3,87\left(1\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(\Rightarrow1,5x+y=0,195\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,09\\y=0,06\end{matrix}\right.\)
\(m_{Al}=0,09\cdot27=2,43g\)
\(m_{Mg}=0,06\cdot24=1,44g\)

Gọi nAl=a mol
nMg=b mol
=>nH2=1,5a+b=1,68/22,4=0,075 mol
mhh cr=mAl+mMg=27a+24b=1,5
=>a=1/3 và b=0,025 mol
=>mAl=0,9gam
=>%mAl=0,9/1,5.100%=60% chọn A
Gọi số mol của Al và Mg lần lượt là x và y
pthh 2Al + 6HCl ---> 2AlCl3 + 3H2
x 1,5 x
Mg + 2HCl ---> MgCl2 + H2
y y
27x + 24y =1,5
ta có hệ phương trình
1,.5x + y =1,68/ 22,4
giải hệ phương trình ta được x= 1/30 , y= 0,025
----> m Al = 1/30 . 27= 0,9 (g)