K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Các câu hỏi dưới đây có thể giống với câu hỏi trên

2 tháng 1 2017
Chọn B.
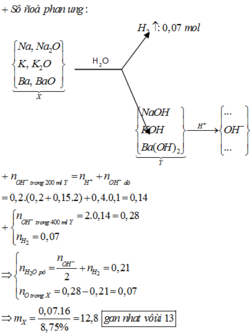
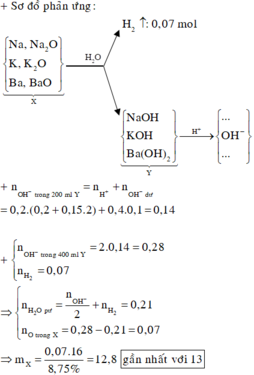
Dung dịch sau có pH = 13 nên sau phản ứng còn dư kiềm: nOH-dư = 0,1.0,4 = 0,04 mol.
⇒ n O H - Y = 0,04+0,2.(0,2+0,2.0,15)=0,14 mol
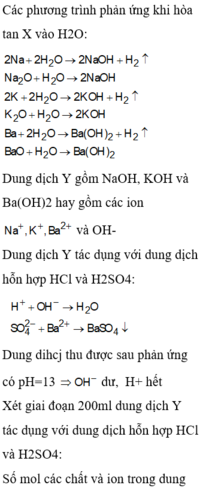
Quy đổi X tương đương với hỗn hợp gồm: Na (x mol), K (y mol), Ba (z mol), O (t mol).
⇒ l6t = 8,75% m.
Theo định luật bảo toàn electron, ta có: x + y + z = 2t + 2 n H 2
⇒ t = (2.0,14 - 2.0,07) : 2 = 0,07 mol ⇒ m = 12,8 ≈ 13 gam.


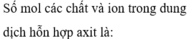
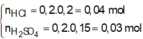
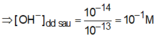
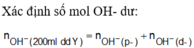
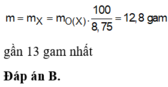

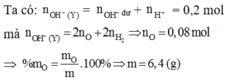
Đáp án : D
nH+ = nHCl + 2nH2SO4 = 0,1 mol
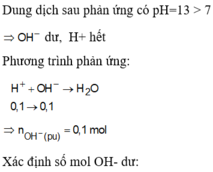
Dung dịch sau có pH = 13 => COH- = 0,1M => nOH- = 0,04 mol
=> nOH (Y) = 0,14 mol = ånKL.(số điện tích)
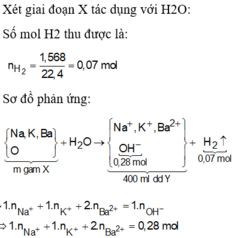
Lại có : 2nH2 = nOH ( do các kim loại tạo ra) = 0,14 mol với 400 ml Y
=> Với 200 ml dung dịch Y có nOH tạo ra do kim loại = 0,07 mol
=> nOH tạo ra do oxit = 0,07 mol = ånKL(oxit).(số điện tích) = 2nO (bảo toàn điện tích)
=> nO = 0,035 mol
Để tạo 400 ml Y thì nO = 0,035.2 = 0,07 mol
=> m = 12,8g