Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nFe = 2. 58/400 = 0,29 mol
nFeSO4 = x , nFe2(SO4)3 = y
⇒mdd = 152 x + 400y = 51,76
nFe = nFeSO4 +2.nFe2(SO4)3 = x+ 2y = 0,29
⇒x= 0,13 mol , y= 0,08 mol
BT S: nH2SO4 = nFeSO4 + 3Fe2(SO4)3 = 0,13 + 3.0,08 = 0,37
⇒b = 0,37.98/9,8% = 370g

Đáp án A
nFe2(SO4)3 = 58/400 = 0,145 mol
nFeSO4 = a ; nFe2(SO4)3 =b
⇒152a + 400b = 51,76
BT Fe: a + 2b = 0,145 . 2 = 0,29 ⇒ a= 0,13 mol; b= 0,08 mol
BT S: nH2SO4 = n FeSO4 + 3nFe2( SO4)3 = 0,13 + 3. 0,08 = 0,37
⇒b= 0,37 .98 /0,098 =370g

Đáp án A
Mg → Mg+2 +2e
Al→ Al+3 +3e
Zn → Zn+2 + 2e
N+5 + 8e → N-3
Muối có Mg(NO3)2, Al(NO3)3, Zn(NO3)2 và NH4NO3 → rắn nung nóng có MgO, ZnO, Al2O3
Đặt khối lượng kim loại trong 19,2 g rắn trên là x g và số mol O là y mol → x + 16y =19,2 mol
Trong muối nitrat của kim loại trong X có nNO3= 2y
Bảo toàn e có nNH4NO3 = y . 2 : 8 = 0,25y
Trong muối khan của dung dịch X có %O = ![]()
Nên x = 12,8 và y =0,4
→ m = x + 62.2y + 80.0,25y =70,4

Đáp án A
Mg → Mg+2 +2e
Al→ Al+3 +3e
Zn → Zn+2 + 2e
N+5 + 8e → N-3
Muối có Mg(NO3)2, Al(NO3)3, Zn(NO3)2 và NH4NO3 → rắn nung nóng có MgO, ZnO, Al2O3
Đặt khối lượng kim loại trong 19,2 g rắn trên là x g và số mol O là y mol → x + 16y =19,2 mol
Trong muối nitrat của kim loại trong X có nNO3= 2y
Bảo toàn e có nNH4NO3 = y . 2 : 8 = 0,25y
Trong muối khan của dung dịch X có %O =
![]()
Nên x = 12,8 và y =0,4
→ m = x + 62.2y + 80.0,25y =70,4

Đáp án A
Hướng dẫn giải :
Mg → Mg+2 +2e Al→ Al+3 +3e Zn → Zn+2 + 2e
N+5 + 8e → N-3
Muối có Mg(NO3)2, Al(NO3)3, Zn(NO3)2 và NH4NO3 → rắn nung nóng có MgO, ZnO, Al2O3
Đặt khối lượng kim loại trong 19,2 g rắn trên là x g và số mol O là y mol → x + 16y =19,2 mol
Trong muối nitrat của kim loại trong X có nNO3= 2y
Bảo toàn e có nNH4NO3 = y . 2 : 8 = 0,25y
Trong muối khan của dung dịch X có %O = ( 2 y + 0 , 25 y ) . 3 , 16 x + 62 . 2 y + 80 . 0 , 25 y . 100 % = 61 , 364 %
Nên x = 12,8 và y =0,4
→ m = x + 62.2y + 80.0,25y =70,4

Đáp án B
Mg, Al, Zn phản ứng với HNO3 không cho sản phẩm khử khí.
⇒ sản phẩm khử duy nhất là NH4NO3.!
⇒ Muối khan gồm Mg(NO3)2, Al(NO3)3, Zn(NO3)2 và NH4NO3.
nhiệt phân muối: R(NO3)n → R2On + NO2 + O2 ||⇒ là thay 2 gốc NO3 bằng 1O trong muối (☆)
Nhiệt phân muối amoni nitrat: NH4NO3 → N2O + 2H2O ||⇒ không thu được rắn.!
Đặt: nNH4NO3 = a mol ⇒ ngốc NO3 trong KL = ne cho = ne nhận = 8nNH4NO3 = 8a mol.
⇒ ∑nNO3 trong muối amoni + kim loại = a + 8a = 9a mol ⇒ ∑nO trong muối trong X = 27a mol
mà oxi chiếm 61,364% về khối lượng ⇒ m = 27a × 32 ÷ 0,61364 = 704a (gam).
lại có mNH4NO3 = 80a (gam) ⇒ mmuối nitrat kim loại = 624a (gam).
Ở (☆) dùng tăng giảm khối lượng ta có: 624a + (4a × 16 – 8a × 62) = 19,2 gam
giải ra a = 0,1 mol thay lại có m = 704a = 70,4 gam.

Đáp án B
Mg, Al, Zn phản ứng với HNO3 không cho sản phẩm khử khí.
⇒ sản phẩm khử duy nhất là NH4NO3.!
⇒ Muối khan gồm Mg(NO3)2, Al(NO3)3, Zn(NO3)2 và NH4NO3.
nhiệt phân muối: R(NO3)n → R2On + NO2 + O2 ||
⇒ là thay 2 gốc NO3 bằng 1O trong muối (¶)
Nhiệt phân muối amoni nitrat: NH4NO3 → N2O + 2H2O ||
⇒ không thu được rắn.!
Đặt: nNH4NO3 = a mol
⇒ ngốc NO3 trong KL = ne cho = ne nhận = 8nNH4NO3 = 8a mol.
⇒ ∑nNO3 trong muối amoni + kim loại = a + 8a = 9a mol
⇒ ∑nO trong muối trong X = 27a mol
mà oxi chiếm 61,364% về khối lượng
⇒ m = 27a × 32 ÷ 0,61364 = 704a (gam).
lại có mNH4NO3 = 80a (gam)
⇒ mmuối nitrat kim loại = 624a (gam).
Ở (¶) dùng tăng giảm khối lượng ta có:
624a + (4a × 16 – 8a × 62) = 19,2 gam
giải ra a = 0,1 mol thay lại có m = 704a = 70,4 gam

Giải thích:
Vì KL + HNO3 không có khí thoát ra => sản phẩm khử là NH4NO3
TQ : 2M(NO3)n ---> M2On + 2nNO2 + 0,5nO2
NH4NO3 ---> N2O + 2H2O
nO(X) = 0,61364m/16 (mol)
nNO3 = ne tđ + nNH4NO3 = 1/3nO(X) = 0,61364m/48 (mol)
Ta có : ne tđ = 8nNH4NO3
=> ne tđ = 0,61364m/54 = nNO2 = 4nO2 ; nNH4NO3 = 0,61364m/432
=> nO2 = 0,61364m/216 (mol)
Bảo toàn khối lượng : mX - mrắn = mNH4NO3 + mNO2 + mO2
=> m – 19,2 = 80. 0,61364m/432 + 46. 0,61364m/54 + 32. 0,61364m/216
=> m = 70,4g
Đáp án B
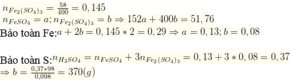
Gọi hóa trị của A là n(n\(\in\)Z;n>0)
\(n_{H_2SO_4}=0,15.0,2=0,03mol\\ A_2O_n+nH_2SO_4\rightarrow A_2\left(SO_4\right)_n+nH_2O\\ \Rightarrow\dfrac{2,4}{2A+16n}=\dfrac{0,03}{n}\Leftrightarrow0,06A+0,48b=2,4n\\ \Leftrightarrow0,06A=2,4n-0,48n\\ \Leftrightarrow0,06A=1,92n\\ \Leftrightarrow A=32n\)
Vậy kim loại A là đồng, Cu
\(n_{CuO}=\dfrac{2,4}{80}=0,03mol\\ CuO+H_2SO_4\rightarrow CuSO_4+H_2\\ n_{CuSO_4}=n_{CuO}=0,03mol\\ m_{CuSO_4}=0,03.160=4,8g\\ CTHH\left(B\right):CuSO_4.xH_2O\\ m_{H_2O.được.ngậm}=7,5-4,8=2,7g\\ \Rightarrow0,03.18x=2,7g\\ \Rightarrow x=5\\ \Rightarrow CTHH\left(B\right):CuSO_4.5H_2O\)