

Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.



Đáp án B
Cách 1: Viết phản ứng, cân bằng hệ số và tính toán theo yêu cầu:
Các phản ứng xảy ra như sau:
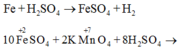
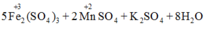
Do đó

Cách 2: Áp dụng phương pháp bảo toàn mol electron:
Ta có: ![]() (bảo toàn nguyên tố Fe)
(bảo toàn nguyên tố Fe)


1,
b1, xd số mol chất khử và chất oxi hóa :
H2SO4 đặc + Al → Al2(SO4)3 + H2S + H2O.
nS= 6 nAl=0 nAl=3 nS=-2
b2, trừ các chất giống nhau từ trái qua phải (lưu ý là phải lấy gt tuyệt đối của hiệu sau khi trừ)
ta được nS=8
nAl=3 (đặt trc các chất bị oxi hóa nhé)
ta được
| 8Al | + | H2SO4 | → | Al2(SO4)3 | + | H2O | + | 3H2S |
b4, đếm từng chất một thôi ,đếm số mol mỗi chất 2 bên cân bằng nhau nhé !
kết quả:
| 8Al | + | 15H2SO4 | → | 4Al2(SO4)3 | + | 12H2O | + | 3H2S |
| (hơi đặc, nóng) | (khí) | |||||||

Fe + H2SO4 → FeSO4 + H2
10FeSO4 + 2KMnO4 + 8H2SO4→ 5Fe2(SO4)3 + K2SO4 + 2MnSO4 + 8H2O
nFeSO4 = 5nKMnO4 = 0,3. 0,2. 5 = 0,3 mol
=> nFe = 0,3 mol <=> mFe = 0,3 .56= 16,8 gam

Bài giải:
Nhớ lại xíu, muối sau pứ bằng tổng khối lượng kim loại cộng khối lượng Cl-
BT hóa trị ta có: 1.nHCl= 2.nH2 nên nHCl= nCl-= 0,5 mol
nên muối sau pứ: mKL + mCl- = 20 + 35,5.0,5 = 37,75(g)