Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Chú ý: Khi đề bài nói làm khô ngoài không khí thì hidroxit không bị chuyển thành oxit. Phải nung nóng thì hidroxit mói bị chuyển thành các oxit tương ứng.

Đáp án D
n h h k h i = 0 , 2 m o l
cho BaCl2 vào kết tủa thu được là BaSO4
n B a S O 4 = 0 , 605 m o l
n H 2 S O 4 = 0 , 605 m o l
n N a O H = 1 , 085 m o l
n N H 3 = 0 , 025 m o l
⇒ n i o n k i m l o a i = 1 , 06 m o l
hỗn hợp khí có chứa H2 nên muối sắt là muối Fe2+
NO3- hết, các muối trung hòa là
MgSO4, FeSO4, K2SO4 và (NH4)2SO4
m F e + m M g = 24,88 gam (1)
nđiện tích - = 2nSO42-= 1,21 mol
nđiện tích += 1,085 + n K +
=> n K + = 0,125 mol
=>nN khí = 0,125 – 0,025 =0,1 mol
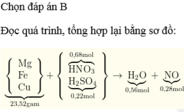
Mặt khác bảo toàn khối lượng
m X + m H 2 S O 4 + m K N O 3 = m m u ố i + m k h í + m H 2 O
=> m H 2 O = 8,91 mol
=> n H 2 O = 0,495 mol
Bảo toàn nguyên tố H có
nH axit = nH ( H 2 O )+ nH ( H 2 ) +nH muối amoni
0,605.2 =0,495.2 +2 n H 2 + 0,025.4
=> n H 2 = 0,06 mol
=> n C O 2 = 0,2 – 0,1 – 0,06 = 0,04 mol
=> n F e C O 3 = 0,04 mol
=> mFe + mMg + m F e 3 O 4 = 26,48 g
m KL (hỗn hợp trên)= 22,64 gam (2)
từ (1) và (2) => mO ( F e 3 O 4 )= 3,84 gam
=> n F e 3 O 4 =0,06 mol
mặt khác vì tổng ion dương kim loại F e 2 + v à M g 2 +
Gọi n F e = a m o l , n M g = b m o l
⇒ 2 a + 2 b = 0 , 2 56 a + 24 b = 12 , 56
⇒ a = 0 , 16 , b = 0 , 15 m o l

Đáp án A
Xử lý hỗn hợp khí X: 3 khí đó
chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2
và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa
N2 và N2O với
MT.bình = 36 = MT.bình cộng của 2 khí.
⇒ nN2 = nN2O
Đặt nNO = a và nN2 = nN2O = b
Ta có hệ:
a + 2b = 0,04
& 30a + 28b + 44b = 1,32
⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận
= 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là
x và y ta có hệ:
(24+17×2).x + (27+17×3)y = 6,42
& 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol
⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ
⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2
= 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15
= 0,345 mol
⇒ mDung dịch HNO3 = 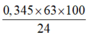
= 90,5625 gam

Đáp án A
Quy hỗn hợp thành Fe2O3, FeO và CuO với số mol lần lượt là a b và c.
Ta có sơ đồ phản ứng:
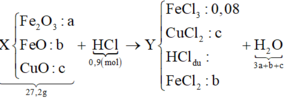
Khi điện phân dung dịch Y đến khi catot thoát khí ⇒ FeCl3 và CuCl2 đã bị điện phân hết.
⇒ mGiảm = nFeCl3×35,5 + nCuCl2×135 = 13,64 gam Û nCuCl2 = 0,08 mol.
⇒ Ta có hệ phương trình
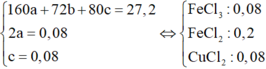
Bảo toàn Clo ⇒ nHCl dư = 0,1 mol.
●Tóm lại sau điện phân dung dịch chứa: nFeCl2 = 0,28 mol và nHCl = 0,1 mol.
Cho dung dịch sau điện phân + AgNO3 ⇒ 3Fe2+ + 4H+ + NO3– → Fe3+ + NO + 2H2O.
⇒ nFe2+ bị mất đi = 0,1 × 3 ÷ 4 = 0,075 mol ⇒ nFe2+ còn lại = 0,28 – 0,075 = 0,205 mol.
⇒ nAg = nFe2+ = 0,205 mol || nAgCl = nCl– = 0,28×2 + 0,1 = mol.
⇒ m↓ = mAg + mAgCl = 0,205×108 + 0,66×143,5 = 116,85

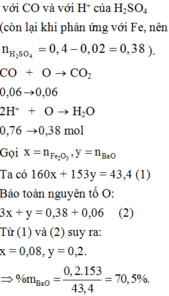

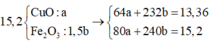
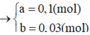
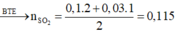


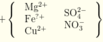

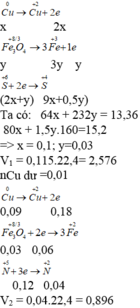
mdd = 10 + 100 + 20 + 0,65 - 0,02 - 2 = 130,43 g.