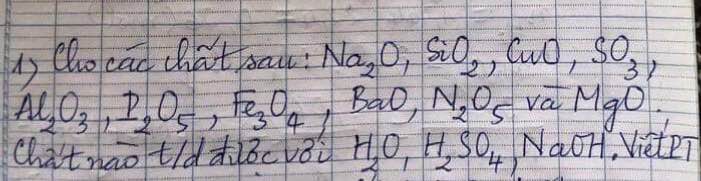Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Quy đổi hỗn hợp X thành \(\left\{{}\begin{matrix}Ba\\Na\\O\end{matrix}\right.\) với nBa = x mol, nNa = y mol và nO = z mol
nH2 = 1,12 :22,4 = 0,05 mol
\(\left\{{}\begin{matrix}Ba\\Na\\O\end{matrix}\right.\) + H2O → \(\left\{{}\begin{matrix}Ba\left(OH\right)_2\\NaOH\end{matrix}\right.\) + H2
Ta có nBa(OH)2 = 20,52: 171 = 0,12 mol
Bảo toàn nguyên tố Ba => x = 0,12 mol
Áp dụng ĐLBT electron và BTKL ta có \(\left\{{}\begin{matrix}y+0,12.2=2z+0,05.2\\0,12.137+23y+16z=21,9\end{matrix}\right.\)
=> y = 0,14 và z = 0,14
a) BTKL => nNaOH = nNa = 0,14 mol
b) nOH- trong dung dịch Y = 0,12.2 +0,14 = 0,38 mol
nCO2 = 6,72:22,4 = 0,3 mol
Ta có \(\dfrac{nOH^-}{nCO_2}\) = 1,26 => tạo 2 muối HCO3- và CO32-
CO2 + OH- → HCO3-
0,3 0,38(dư) 0,3
OH- + HCO3- → CO32- + H2O
0,08 0,3 0,08
CO32- + Ba2+ → BaCO3
0,08 0,12 ---> 0,08
Vậy mBaCO3 = m kết tủa = 0,08.197 = 15,76 gam
Cách 2
\(\left[{}\begin{matrix}Na\\Ba\\Na_2O\\BaO\end{matrix}\right.\) + H2O → \(\left\{{}\begin{matrix}Ba\left(OH\right)_2\\NaOH\left(xmol\right)\end{matrix}\right.\) + H2
Tổng số mol H sau phản ứng = 2nBa(OH)2 + nNaOH + 0,05.2 = (0,34 +x) mol
=> nH2O phản ứng = 0,17 + 0,5x mol
Áp dụng ĐLBT khối lượng => 21,9 + (0,17 + 0,5x).18 = 20,52 + 40x + 0,05.2
=> x = 0,14
Đến đây em giải tiếp tương tự cách 1

nCO2=0,2 mol
GS 25,7 gam muối là muối K2CO3 =>nK2CO3=nCO2=0,2 mol
=>mK2CO3=0,2.138=27,6gam khác 25,7gam=>loại
GS 25,7 gam muối là KHCO3
nKHCO3=nCO2=0,2 mol
=>mKHCO3=100.0,2=20 gam khác 25,7 gam =>loại
Vậy 25,7 gam klg cả 2 muối tạo thành
CO2 +2KOH =>K2CO3 + H2O
x mol =>x mol
CO2 + KOH =>KHCO3
y mol =>y mol
nCO2=x+y=0,2
m muối =138x+100y=25,7
=>x=0,15 và y=0,05 mol
Tính CM dd KOH bạn à
nKOH=0,15.2+0,05=0,35 mol
CM dd KOH=0,35/0,2=1,75M

Bạn ơi chụp rõ đi bạn bạn chụp thế này thì đề thiếu nhiều quá:<

Bảo toàn nguyên tố O :
\(n_{H_2O\left(TN1\right)}=n_{H_2O\left(TN2\right)}=0.08\left(mol\right)\)
Ở TN2, Bảo toàn nguyên tố H :
\(n_H=2\cdot n_{H_2O}=2\cdot0.08=0.16\left(mol\right)\)
Với cùng nồng độ mol thì : tỉ lệ số mol giữa HCl và H2SO4 : \(\dfrac{1}{0.5}=\dfrac{2}{1}\)
\(n_{HCl}=2a\left(mol\right),n_{H_2SO_4}=a\left(mol\right)\)
\(\Rightarrow n_H=2a+a\cdot2=0.16\left(mol\right)\)
\(\Rightarrow a=0.04\)
\(m_{Muối}=m_X+m_{HCl}+m_{H_2SO_4}-m_{H_2O}=5+0.08\cdot36.5+0.04\cdot98-0.08\cdot18=10.4\left(g\right)\)

Tác dụng với \(H_2O:\)\(Na_2O,SO_3,P_2O_5,BaO,N_2O_5,SiO_2\)
Tác dụng với \(H_2SO_4:Na_2O,CuO,Al_2O_3,Fe_3O_4,BaO,MgO\)
Tác dụng với NaOH: \(SiO_2,P_2O_5,N_2O_5,SO_3\)


a,
2Na+2H2O->2NaOH+H2
NaOH+Ca(HCO3)2->NaHCO3+CaCO3+H2O
NaHCO3+NaOH->Na2CO3+H2O
Na2CO3+NaHSO4->NaHCO3+Na2SO4
Na2O+H2O->2NaOH
Na2CO3+Ca(OH)2->2NaOH+CaCO3