
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


PT: \(C+O_2\underrightarrow{t^o}CO_2\) (1)
\(S+O_2\underrightarrow{t^o}SO_2\) (2)
Ta có: mS = 24.0,5% = 0,12 (kg) = 120 (g) ⇒ nS = 120/32 = 3,75 (mol)
Theo PT (2): \(n_{SO_2}=n_S=3,75\left(mol\right)\)
\(\Rightarrow V_{SO_2}=3,75.22,4=84\left(l\right)\)
Ta có: mC = 24 - 0,12 - 24.1,5% = 23,52 (kg) = 23520 (g)
\(\Rightarrow n_C=\dfrac{23520}{12}=1960\left(mol\right)\)
Theo PT (1): \(n_{CO_2}=n_C=1960\left(mol\right)\)
\(\Rightarrow V_{CO_2}=1960.22,4=43904\left(l\right)\)
Sửa: mC = 23,52 (kg) = 23420 (g)
⇒ \(n_C=\dfrac{23520}{12}=1960\left(mol\right)\)
Theo PT (1): \(n_{CO_2}=n_C=1960\left(mol\right)\)
\(\Rightarrow V_{CO_2}=1960.22,4=43904\left(l\right)\)

Bài 1:
Số mol sắt tham gia phản ứng:
nFe = 0,05 mol
a) Thể tích khí hiđro thu được ở đktc:
Fe + 2HCl → FeCl2 + H2.
Theo phương trình hóa học, ta có: nH2 = nFe = 0,05 mol
Thể tích khí thu được ở đktc là: VH2= 22,4 . n = 22,4 . 0,05 = 1,12 lít
b) Khối lượng axit clohiđric cần dùng
Theo phương trình hóa học, ta có:
nHCl = 2nFe = 2 . 0,05 = 0,1 mol
Khối lượng HCl cần dùng là: mHCl = M . n = 0,1 . 36,5 = 3,65 g
Bài 2:
a) Phương trình hóa học của S cháy trong không khí:
S + O2 → SO2
Số mol của S tham gia phản ứng:
nS = 16/32 = 0,05 mol
Theo phương trình hóa học, ta có: nSO2 = nS = nO2 = 0,05 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là:
VSO2= 22,4 . 0,05 = 1,12 lít
Tương tự thể tích khí oxi cần dùng ở đktc là:
VO2 = 22,4 . 0,05 = 1,12 lít
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần là:
=> Vkk = 5 VO2 = 5 . 1,12 = 5,6 lít
Bài 1 :
a) PTPU
Theo pt: nH2 = nFe = 0,05 (mol)
VH2 = 22,4.n = 22,4.0,05 = 1,12 (lít)
b) nHCl = 2.nFe = 2. 0,05 = 0,1 (mol)
mHCl = M.n = 0,1.36,5 = 3,65 (g)
Bài 2 :
a) Phương trình hóa học của S cháy trong không khí:
S + O2 to→→to SO2
b) Số mol của S tham gia phản ứng:
nS = 1,6321,632 = 0,05 mol
- Theo phương trình hóa học, ta có: nSO2nSO2 = nS = 0,05 mol
Thể tích khí sunfurơ sinh ra ở đktc là:
VSO2VSO2 = 22,4 . 0,05 = 1,12 (lít)
- Theo phương trình hóa học, ta có: nO2nO2 = nS = 0,05 mol
Thể tích khí oxi cần dùng ở đktc là:
VO2VO2 = 22,4 . 0,05 = 1,12 (lít)
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần dùng ở đktc là:
Vkk = 5VO2VO2 = 5 . 1,12 = 5,6 (lít)

a)
Gọi hợp chất đó là A
dh/chất/H2 = 81 =) MA = 81 x 2 = 162 (g/mol)
CTHH : CxHyNz
Khối lượng của mỗi nguyên tố có trong 1 mol khí A là :
mC = \(\frac{162\times74,07\%}{100\%}=119,9934\approx120\)
mN = \(\frac{162\times17,28\%}{100\%}=27,9936\approx28\)
mH = \(\frac{162\times8,64\%}{100\%}=13,9968\approx14\)
Số mol nguyên tử của mỗi nguyên tố trong 1mol khí A là
\(n_H=\frac{m}{M}=\frac{14}{1}=14\left(mol\right)\)
\(n_C=\frac{m}{M}=\frac{120}{12}=10\left(mol\right)\)
\(n_N=\frac{m}{M}=\frac{28}{14}=2\left(mol\right)\)
=) Trong 1 mol phân tử hợp chất A có : 14 nguyên tử H , 10 nguyên tử C và 2 nguyên tử N
CTHH là : \(C_{10}H_{14}N_2\)
b) Bạn tự làm nha =)))
Chúc bạn học tốt ![]()

Bài 5: Cho sơ đồ của phản ứng như sau:
Al + CuSO4 → Alx(SO4)y + Cu
a) Xác định các chỉ số x và y.
b) Lập phương trình hóa học và cho biết tỉ lệ số nguyên tử của cặp đơn chất kim loại số phân tử của cặp hợp chất,
Bài 3: Canxi cacbonat là thành phần chính của đá vôi. Khi nung đá vôi xảy ra phản ứng hóa học sau:
Canxi cacbonat → Canxi oxit + cacbon đioxit.
Biết rằng khi nung 280kg đá vôi tạo ra 140kg canxi oxit CaO (vôi sống) và 110kg khí cacbon đioxit CO2.
a) Viết công thức về khối lượng của các chất trong phản ứng.
b) Tính tỉ lệ phần trăm về khối lượng canxi cacbonat chứa trong đá vôi.

Nguyên tử cacbon có số lớp electron như nguyên tử nitơ và nguyên tử neon. (2 lớp e)


Sự cháy trong không khí xảy ra chậm hơn và tạo ra nhiệt độ thấp hơn so với sự cháy trong oxi. Đó là vì trong không khí, thể tích khí nitơ gấp 4 lần khí oxi, diện tích tiếp xúc của chất cháy với các phân tử oxi ít hơn nhiều lần nên sự cháy diễn ra chậm hơn. Một phần nhiệt tiêu hao để đốt nóng khí nitơ nên nhiệt độ đạt được thấp hơn.

Điều kiện cần thiết cho một vật có thể cháy được và tiếp tục cháy được: chất phải nóng đến nhiệt độ cháy, phải đủ khí oxi cho sự cháy.
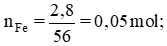

bài mấy?
Bài 1,2,3 bn