Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bảo toàn điện tích → 0,2.1 + 0,1.2 + 0,05.2 = 0,15.1 + 1.x → x = 0,35
Đáp án A

Đáp án D
Để dung dịch tồn tại thì ion Y2- là SO42-
Theo định luật bảo toàn điện tích: 0,1.1+ 0,2.2+0,1.1=0,2+ 2a
Suy ra a= 0,2
Muối khan thu được là: 0,1.39+ 0,2.24+ 0,1.23+0,2.35,5+ 0,2.96= 37,3 gam

Quan sát 4 đáp án ta thấy
![]()
Vì dung dịch tồn tại 0,2 mol Mg2+ mà MgCO3 là chất kết tủa do đó Y sẽ là ![]() . Áp dụng định luật bảo toàn điện tích ta có
. Áp dụng định luật bảo toàn điện tích ta có
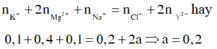
Khối lượng muối bằng tổng khối lượng của các ion trong dung dịch:
![]() gam
gam
Đáp án B.

Đáp án D
BTĐT: nNO3- = nNa+ + 2nBa2+ + 2nMg2+ - nCl- = 0,3.1+0,1.2+0,05.2-0,2.1=0,4 mol
m muối = mNa+ + mBa2+ + mMg2+ + mCl- + mNO3- = 0,3.23+0,1.137+0,05.24+0,2.35,5+0,4.62 = 53,7 gam

Đáp án B
Loại ngay A và D do H+ và CO32- không tồn tại trong cùng 1 dung dịch
Xét B: nK+ + nNH4+ = 0,15 + 0,25 = 0,4 mol; nCl- + 2nCO32- = 0,1 + 2.0,15 = 0,4 mol
=> thỏa mãn định luật bảo toàn điện tích
Xét C: nK+ + 2nMg2+ = 0,15 + 2.0,1 = 0,35 mol; nCl- + 2nSO42- = 0,1 + 2.0,075 = 0,25 mol
=> không thỏa mãn định luật bảo toàn điện tích

Dùng ĐLBT điện tích:
0,4.1+0,05.2= x.2+ y.1
<=> 2x+y= 0,5 (1)
Mà tổng KL muối bằng 35,8 gam:
=> 23.0,4+24.0,05+x.96+62.y= 35,8
<=> 96x+62y=25,4 (2)
Từ (1), (2) ta lập hpt và giải được:x=0,2 ; y=0,1
=> Chọn A

Đáp án B
Theo ĐLBT ĐT thì: 2x+ 0,2.1=0,1+0,4 nên x= 0,15 mol
2H++ CO32- → CO2+ H2O
0,2 0,1
Ba2++ CO32-→ BaCO3
0,15 0,15
nCO3(2-)= 0,25 mol → V= 0,25 lít
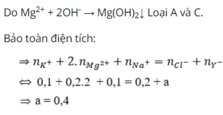

Vì có Mg2+ nên dung dịch không có OH- → Loại B và C
Đáp án A