Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
nH2SO4 = 0,565 mol ; nSO2 = 0,015 mol
+) Phần 1 : Mkhí = 32,8g ; nkhí = 0,0625 mol
Hỗn hợp khí không màu có 1 khí hóa nâu là NO và N2O
=> nNO = 0,05 ; nN2O = 0,0125 mol
Muối thu được là muối sunfat => có S trog D
Qui hỗn hợp D về dạng : Al (x mol) ; O (y mol) ; S (z mol)
Giả sử phản ứng D + HNO3 tạo t mol NH4+
Bảo toàn e : 3nAl + 6nS = 2nO + 3nNO + 8nN2O + 8nNH4
=>3x + 6z = 2y + 0,15 + 0,1 + 8t(1)
Muối sunfat thu được có : NH4+ ; Al3+ ; SO42-
Bảo toàn điện tích : nNH4 + 3nAl = 2nSO4
=>t + 3x = 2z(2)
Khi Cho dung dịch muối này phản ứng với NaOH vừa đủ thì :
Al3+ + 4OH- -> AlO2- + 2H2O
NH4+ + OH- -> NH3 + H2O
=> nNaOH = 4x + t = 0,13(3)
+) Phần 2 : (Al ; O ; S) + O2(không khí) -> ( 0,5x mol Al2O3) + SO2 ↑
=> mgiảm = mS – mO thêm
=>1,36 = 32z – 16.(1,5x – y)(4)
Giải hệ (1,2,3,4) => x = y = 0,03 ; z = 0,05 ; t = 0,01 mol
Vậy D có : 0,02 mol Al2O3 ; 0,02 mol Al ; 0,1 mol S
Bảo toàn e : 2nSO2 + 6nS = 3nAl pứ => nAl pứ = 0,21 mol
nH2SO4 = 3nAl2O3 pứ + (1,5nAl + nSO2 + nS)
=> nAl2O3 = 0,045 mol
Vậy hỗn hợp đầu có : 0,065 mol Al2O3 và 0,23 mol Al
=> m = 12,84g

Đáp án B
Đặt nH2 = x => nH2SO4 = x
BTKL: mKL + mH2SO4 = m muối + mH2
8,975 + 98x = 32,975 + 2x => x = 0,25 mol
=> V = 5,6 lít

Đáp án B
Đặt nH2 = x => nH2SO4 = x
BTKL: mKL + mH2SO4 = m muối + mH2
8,975 + 98x = 32,975 + 2x => x = 0,25 mol
=> V = 5,6 lít

Đáp án B
Ta có: nNaOH = 0,15 mol; nBa(OH)2 = 0,05 mol
Dung dịch Y chứa 0,15 mol Na+, 0,05 mol Ba2+, u mol AlO2- và v mol OH- dư
Định luật bảo toàn điện tích ta có u + v = 0,15 + 0,05.2 = 0,25 (1)
Ta có: nHCl = 0,32 mol và nH2SO4 = 0,04 mol→ nH+ = 0,4 mol; nSO4(2-) = 0,04 mol
→ nBaSO4 = 0,04 mol
Ta có: mkết tủa = 21,02 gam → nAl(OH)3 = 0,15 mol
Nếu Al(OH)3 chưa bị hòa tan thì nH+ = 0,4 = v + 0,15 (2)
Nếu Al(OH)3 đã bị hòa tan thì nH+ = 0,4 = v + 4u - 3.0,15 (3)
Giải hệ (1) và (2) ra vô nghiệm
Giải hệ (1) và (3) ra u = 0,2 và v = 0,05
Vậy Y gồm Na+ 0,15 mol; 0,05 mol Ba2+; 0,2 mol AlO2- và OH- dư (0,05 mol)
V lít dung dịch Z gồm 0,64V mol HCl và 0,08V mol H2SO4
→ nH+ = 0,8V mol và nSO4(2-) = 0,08 V mol
Khi Al(OH)3 max thì 0,8V = u+ v suy ra V = 0,3125
Suy ra nBaSO4 = 0,025 mol → mkết tủa = 21,425 gam
Khi BaSO4 max thì 0,08V = 0,05 suy ra V = 0,625
Suy ra nH+ = 0,8V = v + 4u-3.nAl(OH)3 → nAl(OH)3 = 7/60 mol → mkết tủa = 20,75 gam
Vậy mkết tủa max = 21,425 gam

Chọn đáp án A
n M g = 0 , 15 mol; n Fe = 0 , 1 mol. Ta thấy nếu phản ứng xảy ra vừa đủ thì:
m E = m MgO + m Fe 2 O 3 = 0 , 15 x 40 + 0 , 1 ÷ 2 x 160 = 14 gam < 18 gam.
⇒ A chứa Cu2+ dư ⇒ m CuO = 18 - 14 = 4 gam ⇒ n Cu 2 + dư = n CuO = 0 , 05 mol.
A chứa Mg2+, Fe2+, Cu2+, N O 3 - . Bảo toàn điện tích: n NO 3 - = 0 , 6 mol.
⇒ a + 2 a = 0 , 6 ⇒ a = 0 , 2 mol ⇒ B gồm 0,2 mol Ag và (0,2 – 0,05 = 0,15) mol Cu.
⇒ m = 0,2 × 108 + 0,15 × 64 = 31,2 gam

Đáp án : B
Vì Cu không phản ứng với H2SO4 loãng => mCu = 9,6g => nCu = 0,15 mol
,nH2 = 0,25 mol < nH2SO4 = 0,5 mol
=> axit dư nH+ = 0,5 mol và kim loại tan hết
=> 3nAl + 2nFe = 2nH2 = 0,5 mol và 27nAl + 56nFe = 17,9 – 9,6
=> nAl = nFe = 0,1 mol
,nNaNO3 = 0,12 mol
3Cu + 8H+ + 2NO3- -> 3Cu2+ + 2NO + 4H2O
3Fe2+ + 4H+ + NO3- -> 3Fe3+ + NO + 2H2O
=> sau phản ứng có : 0,15 mol Cu2+ ; 0,1 mol Al3+ ; 0,1 mol Fex+ ; 0,5 mol SO42- ; 0,12 mol Na+ ; 0,02 mol H+
,nNO = nNO3 = 0,12 mol => V = 2,688 lit
Nếu tính lượng muối thì phải loại ra 0,01 mol H2SO4
=> mmuối = 67,7g

Đáp án D
Khí gồm SO2 ; CO2 có n = 0,25 mol và M = 55,2g
=> nSO2 = 0,14 ; nCO2 = 0,11 mol
=> nNa2SO3 = 0,14 ; nCuCO3 = 0,11
Gọi thể tích dung dịch axit là V => nHCl = V ; nH2SO4 = 0,5V mol
=> nH2O =1/2 nH+ = V mol
Bảo toàn khối lượng : mX + maxit = mchất tan + mkhí + mH2O
=> V = 0,33 lit
=> nHCl = 0,33 ; nH2SO4 = 0,165 mol
Bảo toàn điện tích : nNa+ + 2nCu2+ = nCl- + 2nSO4 => nCu2+ = 0,19 mol
=> nCuO = 0,19 – 0,11 = 0,08 mol => m = 37,68g
, nCu2+ đp = 0,19.0,94 = 0,1786 mol
Catot : Cu2+ + 2e -> Cu
Anot : 2Cl- -> Cl2 + 2e
2H2O -> 4H+ + O2 + 4e
=> 2nCu2+ đp = nCl- + nH+ => nH+ = 0,0272 mol
Lấy nFe = 0,0942 mol phản ứng với Z( 0,0272 mol H+ và 0,0114 mol Cu2+)
=> sau phản ứng có : 0,0114 mol Cu và 0,0692 mol Fe dư
=> m1 = 4,6048g
=>D

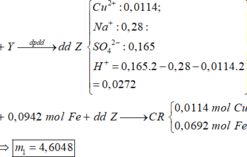
Đáp án B
Bảo toàn nguyên tố Hidro: nH2SO4 = nH2 = 0,25 mol
⇒ mdung dịch H2SO4 = 0,25 × 98 ÷ 0,2 = 122,5(g).
Bảo toàn khối lượng: mdung dịch A = 8,3 + 122,5 – 0,25 × 2 = 130,3(g)