Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

.
Nhận thấy nCO2 = nH2O = 0,4 mol
=> este no đơn chức
=> số C = 0,4 : 0,1 = 4
=> C4H8O2
b.
R1COOR2 + NaOH → R1COONa + R2OH
0,1 → 0,1 0,1
=> Chất rắn gồm R1COONa: 0,1 và NaOH dư: 0,1 mol (m rắn = 13,6g)
=> R1 = 29 (C2H5)
=> X: C2H5COOCH3

· Xét phản ứng của A với NaOH (CaO)
Số mol hidrocacbon = 0,05 mol
CxHyCOOH + NaOH → CxHyCOONa + H2O
CmHn(COOH)2 + 2NaOH → CmHn(COONa)2 + 2H2O
CxHyCOONa + NaOH →Na2CO3 + CxHy+1
CmHn(COONa)2 + 2NaOH →2Na2CO3 + CmHn+2
Vì chỉ thu được 1 hodrocacbon nên
=> x = m và y + 1 = n + 2
=> các axit trong A có chỉ số H bằng nhau
nA = nB = n hidrocacbon = 0,05mol
· Xét phản ứng đốt A:
nCO2 = 0,18 mol ; nH2O = 0,1 mol
=> số C trung bình = 0,18 : 0,05 = 3,6
Số H trung bình = 0,2 : 0,05 = 4
Vì 2 axit có chỉ số H bằng nhau nên
=> y + 1 = n + 2 = 4 => y = 3; n = 2
Mặt khác: m + 1 < 3,6 < m + 2
=> 1,6 < m < 2,6 => m = x = 2
CT của các axit: C2H3COOH → CTCT: CH2=CH–COOH
C2H2(COOH)2 → CTCT: HOOC–CH=CH–COOH ; CH2=C(COOH)2

Ta có M A = 13 x 2 = 26 (gam/mol)
Khi đốt cháy A sinh ra CO 2 , H 2 O → A chứa C, H và không có oxi vì M A = 26 gam/mol.
Gọi công thức của A là C n H m
Phương trình hoá học :
C n H m + (n + m/4) O 2 → n CO 2 + m/2 H 2 O
CO 2 + Ca OH 2 → Ca CO 3 + H 2 O
n A = 5,2/26 = 0,2 mol
n CO 2 = n CaCO 3 = 40/100 = 0,4 mol
Vậy 0,2n = 0,4 => n = 2 => công thức của A là C 2 H 2

Nhận thấy: Đốt cháy A và đốt cháy Y cần thể tích khí O2 là như nhau. Ta có
BTNT C: nCO2 = nCO2 + nNa2CO3 = 0,4
BTKL: mA + mO2 = mCO2 + mH2O
=> mH2O = 7,2g

Biết 1 lít hỗn hợp A ở dạng khí nặng gấp hai lần 1 lít khí C 2 H 6 ở cùng điều kiện.
⇒ n A = n C 2 H 6 ⇒ M A = 2 M C 2 H 6
(cùng điều kiện nên tỉ lệ thể tích chính là tỉ lệ số mol)
Ba chất có cùng công thức phân tử ⇒ có cùng khối lượng mol phân tử : M = 2.30 = 60 (gam/mol). Khi đốt cháy hỗn hợp A thu được CO 2 , H 2 O → công thức phân tử của các chất có dạng C x H y O z
Phương trình hoá học
C x H y O z + (x + y/4 - z/2) O 2 → x CO 2 + y/2 H 2 O
CO 2 + Ca OH 2 → Ca CO 3 + H 2 O
Ta có : n CO 2 = n CaCO 3 = 15/100 = 0,15mol
Theo định luật bảo toàn khối lượng, ta có :
m A + m O = m CO 2 + m H 2 O
⇒ 3 + 7,2 = 0,15 x 44 + m H 2 O ⇒ m H 2 O = 3,6g
n A = 3/60 = 0,05mol; n CO 2 = 0,05x = 0,15 ⇒ x = 3
n H 2 O = 0,05y/2 = 3,6/18 ⇒ y = 8
M A = 12x + y + 16z = 60 ⇒ z = 1 ⇒ ông thức phân tử của A là C 3 H 8 O
Công thức cấu tạo của ba chất là : CH 3 CH 2 CH 2 OH
CH 3 CHOH CH 3
CH 3 -O- CH 2 CH 3

a+b) Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_C=n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\\n_H=2n_{H_2O}=2\cdot\dfrac{5,4}{18}=0,6\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_C=0,2\cdot12=2,4\left(g\right)\\m_H=0,6\cdot1=0,6\left(g\right)\end{matrix}\right.\) \(\Rightarrow m_C+m_H=m_A\)
\(\Rightarrow\) Trong A có Cacbon và Hidro
Xét tỉ lệ \(n_C:n_H=0,2:0,6=1:3\)
\(\Rightarrow\) Công thức phân tử của A là (CH3)n
Vì \(M_A< 40\) \(\Rightarrow\) \(M_A=30\) là hợp lý nhất \(\Rightarrow n=2\)
\(\Rightarrow\) Công thức cần tìm là C2H6 (Etan)
c) Etan không làm mất màu dd Brom
d) PTHH: \(C_2H_6+Cl_2\xrightarrow[]{a/s}C_2H_5Cl+HCl\)

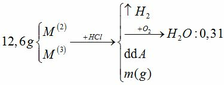
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
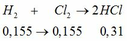
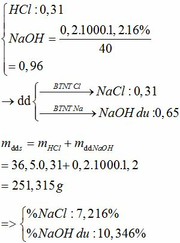

a.

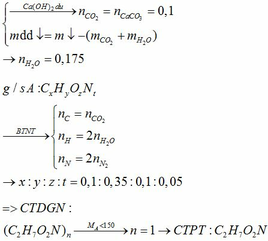
b.
Vì A pứ với NaOH nên CTCT của A là: CH3COONH4 hoặc HCOONH3CH3
Y pứ ở 15000C nên Y là: CH4
=> X: CH3COONa → A:CH3COONH4
Z: CH≡CH → T: CH3CHO
Vậy A là: CH3COONH4 (amoniaxetat)


a) Theo đề ta có:
\(d_{A/H2}=15\)
\(\Rightarrow M_A=15.2=30\left(\frac{g}{mol}\right)\)
Khối lượng của các nguyên tố có trong A là:
\(n_C=n_{CO2}=\frac{8,8}{44}=0,2\left(mol\right)\)
\(\Rightarrow m_C=0,2.12=2,4\left(g\right)\)
\(n_{H2}=n_{H2O}=\frac{5,4}{18}=0,3\left(mol\right)\)
\(\Rightarrow m_{H2}=0,3.2=0,6\left(g\right)\)
\(\Rightarrow m_{O2}=m_A-\left(m_C+m_{H2}\right)=3-\left(2,4+0,6\right)=0\)
Đặt CTTQ của A là: CxHy
Ta có tỉ lệ: \(x:y=n_C:2n_{H2}=0,2:0,6=1:3\)
\(\Rightarrow\) CTN của A là: (CH3)n
Mà 15n ≤ 27
\(\Rightarrow n=2\)
Vậy CTPT của A là: C2H6
b) CTCT của A là:
1/ CH3-CH3
c) \(n_{NaOH}=\frac{60}{40}=1,5\left(mol\right)\)
\(PTHH:CO_2+2NaOH\rightarrow Na_2CO_3+H_2O\)
________0,2/1_0,5/1______________
Tỉ lệ: \(\frac{0,2}{1}< \frac{1,5}{2}\Rightarrow\) NaOH dư
\(\Rightarrow C\%_C=\frac{0,2.106}{19+0,75.40}.100\%=43,3\%\)