
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(a,n_{CO_2}=\dfrac{m_{CO_2}}{M_{CO_2}}=\dfrac{11}{44}=0,25\left(mol\right)\\ b,n_{H_2}=\dfrac{9.10^{23}}{6.10^{23}}=1,5\left(mol\right)\\ V_{H_2\left(đktc\right)}=1,5.22,4=33,6\left(l\right)\)

Bài 2: CTHH của câu d là Na3PO4
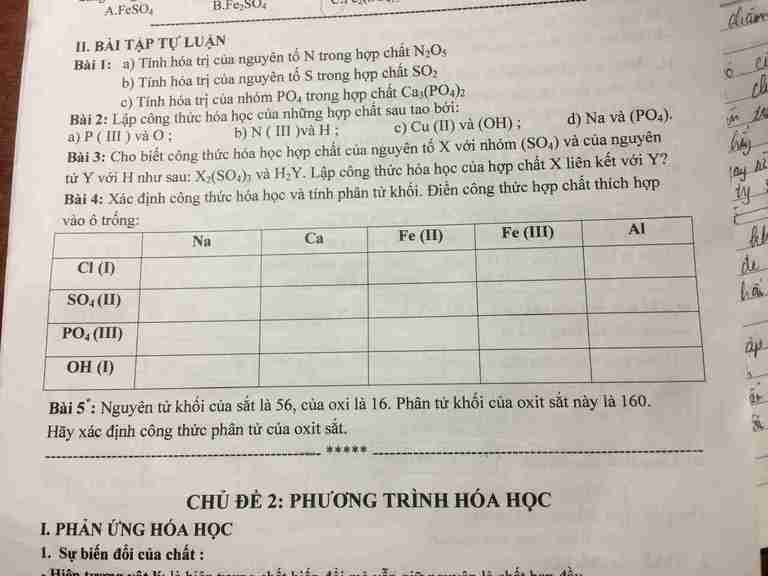
Bài 4:
| Na | Ca | Fe(II) | Fe(III) | Al | |
| Cl(I) | NaCl 58,5 | CaCl2 111 | FeCl2 127 | FeCl3 162,5 | AlCl3 133,5 |
| SO4 (II) | Na2SO4 142 | CaSO4 136 | FeSO4 152 | Fe2(SO4)3 400 | Al2(SO4)3 342 |
| PO4 (III) | Na3PO4 164 | Ca3(PO4)2 310 | Fe3(PO4)2 358 | FePO4 151 | AlPO4 122 |
| OH (I) | NaOH 40 | Ca(OH)2 74 | Fe(OH)2 90 | Fe(OH)3 107 | Al(OH)3 78 |

Câu 3 :
Số mol của sắt
nFe = \(\dfrac{m_{Fe}}{M_{Fe}}=\dfrac{5,6}{56}=0,1\left(mol\right)\)
Pt : Fe + H2SO4 → FeSO4 + H2\(|\)
1 1 1 1
0,1 0,1 0,1 0,1
a) Số mol của khí hidro
nH2 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,1 . 22,4
= 2,24 (l)
b) Số mol của muối sắt (II) sunfat
nFeSO4 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
Khối lượng của muối sắt (II) sunfat
mFeSO4 = nFeSO4 . MFeSO4
= 0,1 . 152
= 15,2 (g)
c) Số mol của dung dịch axit sunfuric
nH2SO4 = \(\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
200ml = 0,2l
Nồng độ mol của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}=\dfrac{0,1}{0,2}=0,5\left(M\right)\)
Chúc bạn học tốt
Câu 4 :
Số mol của photpho
nP = \(\dfrac{m_P}{M_P}=\dfrac{6,2}{31}=0,2\left(mol\right)\)
Pt : 4P + 5O2 → (to) 2P2O5
4 5 2
0,2 0,25 0,1
a) Số mol của đi photpho pentaoxit
nP2O5 = \(\dfrac{0,2.2}{4}=0,1\left(mol\right)\)
Khối lượng của đi photpho pentaoxit
mP2O5 = nP2O5 . MP2O5
= 0,1 . 142
= 14,2 (g)
b) Số mol của khí oxi
nO2 = \(\dfrac{0,2.5}{4}=0,25\left(mol\right)\)
Thể tích của khí oxi ở dktc
VO2 = nO2 . 22,4
= 0,25 . 22,4
= 5,6 (l)
c) Pt : CH4 + 2O2 → CO2 + 2H2O\(|\)
1 2 1 2
0,25 0,125
Số mol của khí cacbonic
nCO2 = \(\dfrac{0,25.1}{2}=0,125\left(mol\right)\)
Thể tích của khí cacbonic ở dktc
VCO2 = nCO2 . 22,4
= 0,125 . 22,4
= 2,8 (l)
Chúc bạn học tốt

Bài 1
Chọn hệ số và CTHH thích hợp đặt vào những chỗ có dấu chấm hỏi trong các phương trình hóa học sau:
a) ? Na + ? → 2 Na2O
b) ? CuO + ?HCl → CuCl2 + ?
c) Al2(SO4)3 + ? BaCl2 → ? AlCl3 + ?
d) ? Al(OH)3 → Al2O3 + ?
Bài 2
Chọn hệ số và CTHH thích hợp đặt vào những chỗ có dấu chấm hỏi trong các phương trình hóa học sau:
a) ? CaO + ? HCl → CaCl2 + ?
b) ?Al + ? → 2Al2O3
c) FeO + CO → ? + CO2
d) ?Al + ?H2SO4 →Al2(SO4)3 + ?H2
e) BaCl2 + ?AgNO3 →Ba(NO3)2 + ?
f) Ca(OH)2 + ?HCl → ? + 2H2O
g) 3Fe3O4 + ?Al → ?Fe + ?
h) Ca(OH)2 + CO2 → ? + H2O
i) Ca(HCO3)2 → CaCO3 + CO2 + ?
Bài 3
Lập các PTHH sau và cho biết tỉ lệ số nguyên tử / phân tử của chất phản ứng với sản phẩm.
a) CuO + Cu → Cu2O
b) FeO + O2 → Fe2O3
c) Fe + HCl → FeCl2 + H2
d) Na + H2SO4 → Na2SO4 + H2
e) NaOH + CuSO4 → Cu(OH)2 + Na2SO4
f) Na2CO3 + Ca(OH)2 → CaCO3 + NaOH
g) Fe(OH)3 → Fe2O3 + H2O
h) CaO + HNO3 → Ca(NO3)2 + H2O
i) Fe(OH)x + H2SO4 → Fe2(SO4)x + H2O

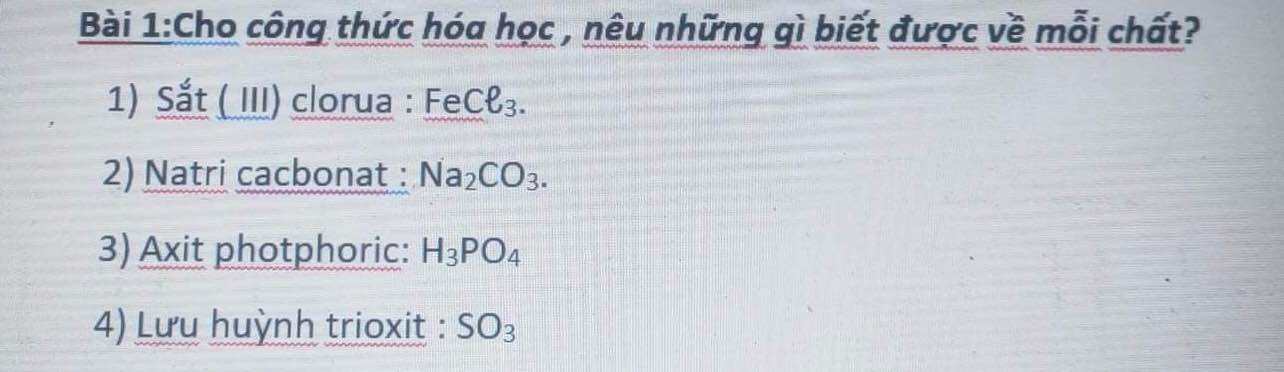
1.
- Hợp chất cấu tạo từ 2 nguyên tố: Fe và Cl
- Hợp chất có: 1 nguyên tố Fe và 3 nguyên tố Cl
- \(PTK=56+35,5\text{ x }3=162,5\left(đvC\right)\)
===========
2.
- Hợp chất cấu tạo từ 3 nguyên tố: Na, C và O
- Hợp chất có: 2 nguyên tố Na, 1 nguyên tố C và 3 nguyên tố O
- \(PTK=23\text{ x }2+12+16\text{ x }3=106\left(đvC\right)\)
==========
3.
- Hợp chất cấu tạo từ 3 nguyên tố: H, P và O
- Hợp chất có: 2 nguyên tố H, 1 nguyên tố P và 4 nguyên tố O
- \(PTK=1\text{ x }3+31+16\text{ x }4=98\left(đvC\right)\)
==========
4.
- Hợp chất cấu tạo từ 2 nguyên tố: S và O
- Hợp chất có: 1 nguyên tố S và 3 nguyên tố O
- \(PTK=32+16\text{ x }3=80\left(đvC\right)\)

Số p+số e+số n=28
Số n=28*35.7%=10
->Số p+số e=28-10=18
Mà số p=số e
->Số p= số e=9
-> X là Flo

Ở $20^oC$,
300 gam nước hòa tan 108,6 gam NaCl thu được dung dịch bão hòa
Suy ra :
100 gam nước hòa tan x gam NaCl thu được dung dịch bão hòa
$\Rightarrow x = \dfrac{100.108,6}{300} = 36,2(gam)$
$\Rightarrow S_{NaCl} = 36,2(gam)$
b)
$S_{AgNO_3} = 222(gam)$, tức là :
222 gam $AgNO_3$ tan tối đa trong 100 gam nước tạo thành dung dịch bão hòa
Suy ra:
y gam $AgNO_3$ tan tối đa trong 250 gam nước tạo thành dung dịch bão hòa
$\Rightarrow y = \dfrac{250.222}{100} = 2,50222(gam)$

2Al+3H2SO4->Al2(SO4)3+3H2
0,2-----0,3-------0,1------------0,3
n Al=\(\dfrac{5,4}{27}\)=0,2 mol
n H2SO4= \(\dfrac{30}{98}\)=0,306 mol
=>H2SO4 còn dư
=>VH2=0,3.22,4=6,72l
=>m Al2(SO4)3=0,1.342=34,2g
=>m H2SO4 dư=0,006.98=0,588g
\(n_{Al}=\dfrac{m_{Al}}{M_{Al}}=\dfrac{5,4}{27}=0,2mol\)
\(n_{H_2SO_4}=\dfrac{m_{H_2SO_4}}{M_{H_2SO_4}}=\dfrac{30}{98}=\dfrac{15}{49}mol\)
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
2 3 1 3 ( mol )
0,2 15/49 ( mol )
Ta có: \(\dfrac{0,2}{2}< \dfrac{15}{49}:3\)
=> Chất còn dư là \(H_2SO_4\)
\(V_{H_2}=n_{H_2}.22,4=\left(\dfrac{0,2.3}{2}\right).22,4=6,72l\)
\(m_{Al_2\left(SO_4\right)_3}=n_{Al_2\left(SO_4\right)_3}.M_{Al_2\left(SO_4\right)_3}=\left(\dfrac{0,2.1}{2}\right).342=34,2g\)
\(m_{H_2SO_4\left(du\right)}=n_{H_2SO_4\left(du\right)}.M_{H_2SO_4}=\left(\dfrac{15}{49}-\dfrac{0,2.3}{2}\right).98=0,6g\)

Số hạt mang điện là:
34 : (11 + 6) . 11 = 22 (hạt)
Số proton của X là:
22 : 2 = 11 (hạt)
Số hạt mang điện là:
34 : (11 + 6) . 11 = 22 (hạt)
Số proton của X là:
22 : 2 = 11 (hạt)



Bài 3:
a, PTHH: Mg + 2HCl \(\rightarrow\) MgCl2 + H2
b, \(n_{Mg}=\dfrac{7,2}{24}=0,3mol\)
\(n_{MgCl_2}=0,3.1=0,3mol\\ \Rightarrow m_{MgCl_2}=0,3.95=28,5g\)
c, \(n_{H_2}=0,3.1=0,3mol\\ \Rightarrow V_{H_2}=0,3.22,4=6,72l\)
Bài 4:
a, PTHH: Zn + 2HCl \(\rightarrow\) ZnCl2 + H2
b,
\(n_{Zn}=\dfrac{13}{65}=0,2mol\\ \Rightarrow n_{ZnCl_2}=0,2.1=0,2mol\\ m_{ZnCl_2}=0,2.136=27,2g\)
c, \(n_{H_2}=0,2.1=0,2mol\\ \Rightarrow V_{H_2}=0,2.22,4=4,48l\)