Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

* Số mol của H 2 S O 4 cần để pha chế 500ml dung dịch H 2 S O 4 1M:
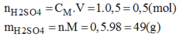
* Khối lượng H 2 S O 4 98% có chứa 49g H 2 S O 4 :
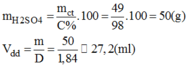
* Cách pha chế: Đổ khoảng 400ml nước cất vào cốc có chia độ có dung tích khoảng 1lit. Rót từ từ 27,2ml H 2 S O 4 98% vào cốc khuấy đều. Sau đó thêm dần dần nước cất vào cốc cho đủ 500ml. ta pha chế được 500ml dung dịch H 2 S O 4 1M.

Pha chế 50ml dung dịch C u S O 4 1M
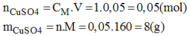
* Cách pha chế:
Cân 8g C u S O 4 cho vào bình. Cho thêm từ từ nước cất vào bình và khuấy đều cho muối tan đến khi đủ 50ml. Ta được 50ml dung dịch C u S O 4 có nồng độ 1M

Gọi số ml dd HCl ở lọ 1 và 2 lần lượt là:a;b(ml)
V của dd HCl 1M là:a
V của dd HCl 3M là:3b
Ta có:
CM=\(\dfrac{a+3b}{a+b}=2\)(a+b=50)
\(\Leftrightarrow a+3b=100\)
\(\Leftrightarrow2b=50\)
\(\Leftrightarrow b=25\)
\(\Rightarrow a=25\)
Vậy để pha chế 50 ml dd HCl 2M thì ta cần đổ 25ml dd HCl 1M và 25ml dd HCl 3M
Gọi a, b lần lượt là thể tích dung dịch HCl của lọ thứ 1và lọ thứ 2 (a, b > 0 , lít)
=>: \(a+b=0,05\left(I\right)\)
Ta có: \(n_{HCl}\)(lọ 1) \(=a.1=a\left(mol\right)\)
\(n_{HCl}\)(lọ 2) \(=3b\left(mol\right)\)
\(n_{HCl}\left(sau\right)=2.0,05=0,1\left(mol\right)\)
\(\Rightarrow a+3b=0,1\left(II\right)\)
Từ (I) và (II) \(\Rightarrow\left\{{}\begin{matrix}a=0,025\left(lit\right)=25\left(ml\right)\\b=0,025\left(lit\right)=25\left(ml\right)\end{matrix}\right.\)
Vậy....

1) Thực hành 1
Phần tính toán
Khối lượng chất tan (đường) cần dùng là:
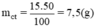
Khối lượng nước cần dùng là: 50 - 7,5 = 42,5(g).
Phần thực hành:
Cần 7,5g đường khan cho vào cốc có dung tích 100ml, khuấy đều với 42,5g nước, được 50g dung dịch đường 15%.
2) Thực hành 2
Phần tính toán
Số mol NaCl cần dùng là:
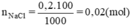
Có khối lượng là: 58,5 x 0,02 = 1,17(g).
Phần thực hành:
Cho 1,17g NaCl khan cho vào cốc chia độ. Rót từ từ nước vào cốc và khuấy đều đến cho vạch 100ml, được 100ml dung dịch NaCl 0,2M.
3) Thực hành 3
Phần tính toán
Khối lượng chất tan(đường) có trong 50g dung dịch đường 5% là:
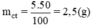
Khối lượng dung dịch đường 15% có chứa 2,5g đường là:
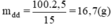
Khối lượng nước cần dùng là: 50 - 16,7 = 33,3(g).
Phần thực hành:
Cần 16,7g dung dịch đường 15% cho vào cốc có dung tích 100ml.Thêm 33,3g nước (hoặc 33,3ml) vào cốc, khuấy đều, được 50g dung dịch đường 5%.
4) Thực hành 4
Phần tính toán
Số mol chất tan (NaCl) có trong 50ml dung dịch 0,1M cần pha chế là:
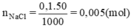
Thể tích dung dịch NaCl 0,2M trong đó có chứa 0,005mol NaCl là:
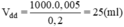
Phần thực hành:
Đong 25ml dung dịch NaCl 0,2M cho vào cốc chia độ. Rót từ từ nước vào cốc đến vạch 50ml. Khuấy đều, được 50ml dung dịch NaCl 0,1M.

Câu 1 :
Trong 150 ml dung dịch HCl 10% có D = 1,047 g/ml có:
m dd HCl = D.V = 150.1,047 = 157,05(gam)
n HCl = 157,05.10%/36,5 = 0,43(mol)
Trong 250 ml dung dịch HCl 2M có :
n HCl = 0,25.2 = 0,5(mol)
Sau khi trộn :
n HCl = 0,43 + 0,5 = 0,93(mol)
V dd = 150 + 250 = 400(ml) = 0,4(lít)
Suy ra :CM HCl = 0,93/0,4 = 2,325M
Đáp án C

bài 3:a) nCaCO3 = 0,07 mol
CaCO3 + 2HNO3 ---> Ca(NO3)2 + H2O + CO2
0.07.........0.14
=> nHNO3 trong Z là 0,14*2 = 0,28 mol
=> CM Z = 0,28/(0,3+0,2) = 0,56 M
gọi CM dd Y = b M; CM dd X = a M
nHNO3 trong X = 0,2*a mol
=> nHNO3 trong Y = 0,3*b mol
X điều chế từ Y nghĩa là từ dd Y ta có thể điều chế một dd có nồng độ mol/lit giống Y
=> đặt V dd Y đạ dùng để điều chế X là V (lit)
=> CM X' = nHNO3/(V H2O + V dd Y)
hay = b* V/(V+3V) = a
=> 4a = b
mà theo câu a ta lại có :
n HNO3 trong X + nHNO3 trong Y = 0,2*a + 0,3*b = 0,28
giải hệ ta đk; x = 0,2M
y = 0,8M

a, _Đánh STT cho các lọ_
- Cho que đóm còn đang cháy vào từng lọ:
+ Cháy mãnh liệt hơn: O2
+ Cháy màu xanh nhạt: H2
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
+ Vụt tắt: CO2
b, \(C\%_{NaCl}=\dfrac{40}{40+120}.100\%=25\%\)
a.Đưa que đóm đỏ vào 3 lọ:
-O2: qua đóm cháy mãnh liệt
-H2: qua đóm cháy với ngọn lửa xanh, nổ nhẹ
-CO2: qua đóm vun tắt đi
b.\(m_{dd}=40+120=160g\)
\(C\%_{NaCl}=\dfrac{40}{160}.100\%=25\%\)

số mol của dd HCL 10% là:
nHCL=(C%.mdd)/(100.M)=(10.150.1.0,47)/(100.36,5)~0,43 (mol)
số mol của dd HCL 2M là:
nHCl=CMCM.V=2.0,25=0,5(mol)
nồng đọ mol của dd HCL thu đc là:
CmCmHCL=n/V=(0,43+0,5)/(0,15+0,25)=2,3(M)
vậy dung dịch mới thu được có nồng độ mol là 2,3M


Pha chế 50ml dung dịch H 2 S O 4 1,5M.
- Số mol H 2 S O 4 cần pha chế 50ml dung dịch H 2 S O 4 1,5M:
n H 2 S O 4 = CM.V = 1,5.0,05 = 0,075 (mol)
Gọi x(ml) là thể tích của dung dịch H 2 S O 4 1M (1)
Gọi y(ml) là thể tích của dung dịch H 2 S O 4 3M (2)
Giải hệ phương trình ta có: x = 37,5ml; y = 12,5ml
- Cách pha chế:
+ Đong lấy 37,5ml dung dịch H 2 S O 4 1M và 12,5ml dung dịch H 2 S O 4 3M cho vào bình, lắc đều, ta được 50ml dung dịch H 2 S O 4 1,5M.