Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A.
Phân tích đồ thị:
+ Đoạn 1: 3Ba(OH)2 + Al2(SO4)3 ![]() 2Al(OH)3 + 3BaSO4.
2Al(OH)3 + 3BaSO4.
+ Đoạn 2: 3Ba(OH)2 + 2AlCl3 ![]() 2Al(OH)3 + 3BaCl2.
2Al(OH)3 + 3BaCl2.
+ Đoạn 3: Ba(OH)2 + 2Al(OH)3 ![]() Ba(AlO2)2 + 4H2O.
Ba(AlO2)2 + 4H2O.
+ Đoạn 4: không còn phản ứng
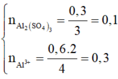
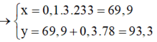
![]()

Đáp án C
+ Tại n = 0,55 mol: BaSO4 đạt cực đại
nBa2+ = nSO42- => 0,55 = 3a + b
+ Tại n = 0,3 mol: Al(OH)3 bắt đầu bị hòa tan khiến cho lượng kết tủa tăng chậm lại
nOH- = 3nAl3+ => 2.0,3 = 3.2a => a = 0,1
=> b = 0,25
=> a : b = 2 : 5

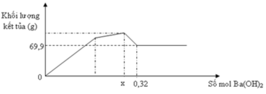
Tại n Ba ( OH ) 2 = 0 , 32 mol thì lượng kết tủa ổn định sau khi đã giảm
→ lúc này OH hòa tan hết Al(OH)3
Lượng kết tủa chỉ có BaSO4: 0,3 mol
Ta có: 4OH−+Al3+→AlO2−+2H2O
→ n Al 3 + = 0 , 16 mol
Tại vị trí gấp khúc đầu tiên: đồ thì tăng chậm hơn giai đoạn đầu
→ chứng tỏ lúc này có sự hòa tan Al(OH)3 nhưng lượng kết tủa tăng vì đang tạo thêm BaSO4
Giai đoạn đầu tăng đều vì có sự tăng đồng thời Al(OH)3 và BaSO4
Đến n Ba ( OH ) 2 = x thì lượng BaSO4 tối đa và chỉ còn sự tan Al(OH)3dẫn đến đồ thị đi xuống
→ x = n BaSO 4 = 0 , 3 mol
Đáp án C

Đáp án B
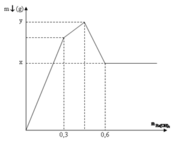
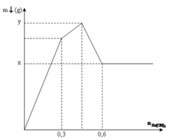
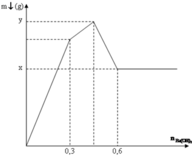
Tại điểm 0,6 mol Ba(OH)2: Al(OH)3 tan hết
![]()
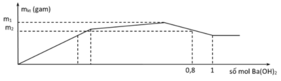
Tại điểm H kết tủa Al(OH)3 đạt cực đại nên ![]()
Tại điểm 0,3 mol Ba(OH)2 thì n S O 4 2 - hết nên n S O 4 2 - = 0,3 mol
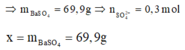
![]()
= 93,3 g
x+ y = 163,2 g

Đáp án B
Nhận thấy tại thời điểm 0,3 mol thì Ba(OH)2 kết tủa vừa đủ với Al2(SO4)3
Khi đó kết tủa gồm BaSO4 : 0,3 mol và Al(OH)3 : 0,2 mol
→ nAl2SO4 = 0,3 : 3= 0,1 mol
Tại thời điểm 0,6 mol Ba(OH)2 thì kết tủa chỉ còn BaSO4 : 0,1 mol, toàn bộ lượng Al(OH)3 bị hòa tan hết → x = 0,3. 233= 69,9 gam
→ 4∑nAl3+ = nOH- = 0,6.2 = 1,2 → ∑nAl3+ = 0,3 mol
Vậy kết tủa cực đại gồm BaSO4 : 0,3 mol và Al(OH)3 : 0,3 mol
→ y = 0,3. 233+ 0,3. 78= 93,3 gam
→ x+ y = 69,9 + 93,3 = 163,2 gam

Đáp án B
Tại điểm 0,6 mol Ba(OH)2: Al(OH)3 tan hết
![]()
Tại điểm H kết tủa Al(OH)3 đạt cực đại nên
![]()
Tại điểm 0,3 mol Ba(OH)2 thì S O 4 2 - hết nên n S O 4 2 - = 0 , 3 m o l
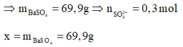
![]()
= 69,9 + 78.0,3 = 93,3 g
x+ y = 163,2 g

Đáp án A
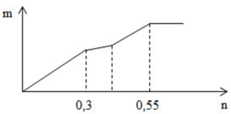
Ta thấy đồ thị được hình thành bởi 3 đường: (1) là kết tủa tạo thành khí Al2(SO4)3 phản ứng với Ba(OH)2 ; (2) là kết tủa tạo thành khi AlCl3 phản ứng với Ba(OH)2 ; (3) là kết tủa Al(OH)3 sinh ra bị hòa tan hết.


Đáp án D
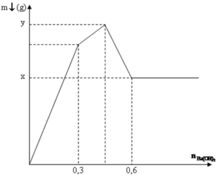
GĐ 1: Kết tủa tăng mạnh nhất do vừa tạo thành BaSO4 và Al(OH)3
GĐ 2: Kết tủa BaSO4 đạt cực đại nên lượng kết tủa tăng chậm đi
GĐ 3: Al(OH)3 bắt đầu bị hòa tan nên lượng kết tủa giảm
nAl2(SO4)3 = x
nAlCl3 = y
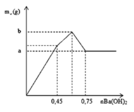
+ Tại nBa(OH)2 = 0,45 mol thì BaSO4 đạt cực đại
nSO42- = nBa(OH)2 => 3x = 0,45
=> x = 0,15
+ Tại nBa(OH)2 = 0,75 mol thì Al(OH)3 vừa bị hòa tan hết
nOH- = 4nAl3+ => 0,75.2 = 4.(2.0,15 + y)
=> y = 0,075 mol
a = mBaSO4 max = 0,45.233 = 104,85 gam
b = mBaSO4 max + mAl(OH)3 max = 104,85 + 78(2.0,15 + 0,075) = 134,1 gam
=> a + b = 104,85 + 134,1 = 238,95 gam

Giải thích:
GĐ 1: Kết tủa tăng mạnh nhất do vừa tạo thành BaSO4 và Al(OH)3
GĐ 2: Kết tủa BaSO4 đạt cực đại nên lượng kết tủa tăng chậm đi
GĐ 3: Al(OH)3 bắt đầu bị hòa tan nên lượng kết tủa giảm
nAl2(SO4)3 = x
nAlCl3 = y
+ Tại nBa(OH)2 = 0,45 mol thì BaSO4 đạt cực đại
nSO42- = nBa(OH)2 => 3x = 0,45 => x = 0,15
+ Tại nBa(OH)2 = 0,75 mol thì Al(OH)3 vừa bị hòa tan hết
nOH- = 4nAl3+ => 0,75.2 = 4.(2.0,15 + y) => y = 0,075 mol
a = mBaSO4 max = 0,45.233 = 104,85 gam
b = mBaSO4 max + mAl(OH)3 max = 104,85 + 78(2.0,15 + 0,075) = 134,1 gam
=> a + b = 104,85 + 134,1 = 238,95 gam
Đáp án D


Đặt số mol Al2(SO4)3 là x; AlCl3 là 3x
Khi đường kết tủa đi ngang, là khi Al(OH)3 tan hoàn toàn, tạo thành Al(OH)4− và lúc đó chỉ còn BaSO4
nOH− = 4.(2x + 3x) = 1.2 → x = 0,1 mol
Khi kết tủa cực đại, nOH− = 3.(2x+3x) = 1,5 mol:
Đáp án D