Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Bạn tham khảo
Bài 1: Cân bằng phản ứng oxi hóa – khử ( bằng phương pháp thăng bằng electron) sau và cho biết chất khử, chất oxi hóa, quá trình khử, quá trình oxi hóa ở mỗi p

a,
Fe+2HCl → FeCl2+H2
H2+Cl2 → 2HCl
MnO2+4HCl → MnCl2+Cl2+2H2O
Cu+Cl2 → CuCl2
CuCl2+2KOH → Cu(OH)2+2KCl
Cu(OH)2+H2SO4 → CuSO4+2H2O
CuSO4+2KOH → K2SO4+Cu(OH)2
K2SO4+2AgNO3 → Ag2SO4+2KNO3
b,
FeS+2HCl → FeCl2+H2S
2H2S+SO2 → 3S+2H2O
2Na+S → Na2S
Na2S+ZnCl2 → ZnS+2NaCl
ZnS+H2SO4 → ZnSO4+H2S
S+O2 → SO2
2SO2+O2 ⇌ 2SO3
SO3+H2O → H2SO4
c,
SO2+2H2S → 3S+2H2O
Fe+Sto → FeS
FeS+2HCl → FeCl2+H2S
2NaOH+H2S → Na2S+2H2O
Na2S+Pb(NO3)2 → PbS+2NaNO3
d,
4FeS2+11O2 → 2Fe2O3+8SO2
SO2+2H2S → 3S+2H2O
H2+S → H2S
H2S+4Br2+4H2O → 8HBr+H2SO4
H2SO4+NaCl → NaHSO4+HCl
MnO2+4HCl → MnCl2+Cl2+2H2O
3Cl2+6KOH → 5KCl+KClO3+3H2O
2KClO3 → 2KCl+3O2
e,
H2+S → H2S
2H2S+3O2 → 2H2O+2SO2
SO2+O2 → SO3
SO3+H2O → H2SO4
2NaCl+H2SO4 → Na2SO4+2HCl
2HCl → Cl2+H2

1. Hãy giải thích tại sao nước của H2S để lâu trong kk bị vấn đục. Viết pt hóa học minh họa.
H2S+H2O->H2O+S
2. Vì sao các đồ vật bằng bạc để lâu ngày trong kk bị xám đen.
vì chúng td với H2S
H2S+Ag+O2->Ag2S+h2O
3. Xác định số oxi hóa của lưu huỳnh trong các chất sau: H2S, SO2, H2SO4, S
H2S=>Sht: -2
, SO2=>S:+4
, H2SO4=>S+6
, S=>S:+0
1) Dung dịch H2S để lâu ngày bị vẩn đục do bị O2 trong không khí oxi hoá giải phóng ra không tan trong nước
2H2S+O2 => 2S↓+2H2O
2)Do bạc tác dụng với khí O2 và H2S có trong không khí tạo ra bạc sunfua (Ag2S) màu đen.
4 Ag + O2 + 2 H2S => 2Ag2S + 2 H2O
Khi bạc sunfua gặp nước sẽ có một lượng rất nhỏ đi vào nước thành ion Ag+. Ion Ag+ có tác dụng diệt khuẩn rất mạnh, chỉ cần 1/5 tỉ gam bạc trong 1 lít nước cũng đủ diệt vi khuẩn. Không cho vi khuẩn phát triển nên giữ cho thức ăn lâu bị ôi thiu.
3)0, –2, +6, +4.

Đáp án C.
(1) H2S + 4Cl2 + 4H2O → H2SO4 + 8HCl
(3) SO2 + Br2 + 2H2O → 2HBr + H2SO4
(5) S + 3F2 → SF6
(6) 2SO2 + O2 →2SO3

Khi S phản ứng với các đơn chất có độ âm điện lớn hơn sẽ thể hiện tính khử
Do đó phản ứng (1) và (3), S đóng vai trò chất khử

a, 4FeS2+11O2--- > 8SO2+2Fe2O3
2SO2+O2--- > 2SO3
SO3+H2O--- > H2SO4
2H2SO4đ+Cu--- > SO2+CuSO4+2H2O
SO2+2H2S--- >3S+2H2O
S+Fe--- >FeS
FeS+2HCl--- > H2S+FeCl2
2H2S+3O2--- > 2SO2.+2H2O
b, 2H2S+SO2--- >3S+2H2O
S+H2--- > H2S
2H2S+3O2--- > 2SO2+2H2O
SO2+BaO--- > BaSO3
BaSO3+2HCl--- > SO2+BaCl2+H2O
2SO2+O2+2H2O-- > 2H2SO4
H2SO4+Ba--- > BaSO4+H2
c, 2H2S+3O2--- > 2SO2+2H2O
2SO2+O2--- > 2SO3
S+O2--- > SO2
SO3+H2O--- > H2SO4
2H2SO4đ+Cu--- > SO2+CuSO4+2H2O
SO2+2H2S--- > S+2H2O
d,. FeS+2HCl--- > H2S+FeCl2
(1)2H2S+SO2--- > 2S+2H2O
S+O2 --- > SO2
2SO2+O2-->2SO3
(1) SO3+H2O--- > H2SO4
H2SO4+CuO--- > CuSO4+H2O
CuSO4+BaCl2--- > CuCl2+BaSO4
(1) --- > SO2 --- > HBr

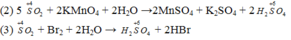

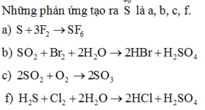
Đáp án C.
FeS + 2HCl→ FeCl2 + H2S
2H2S + 3O2 → 2SO2 + 2H2O