Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đề bài này đủ dữ kiện em nhé.
Vì trong đề có nói là nFeO=nFe2O3. Suy ra quy đổi hỗn hợp FeO, Fe2O3, Fe3O4(FeO.Fe2O3 tỉ lệ 1:1) về thành hỗn hợp của FeO và Fe2O3 với số mol bằng nhau

Fe3O4 + 8HCl --> FeCl2 + 2FeCl3 + 4H2O
_a_______8a______a_____2a______4a_
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
_b______6b_______2b_____3b_
FeO + 2HCl --> FeCl2 + H2O
_c____2c_______c______c_
Fe + 2HCl --> FeCl2 + H2
_d___2d________d________d_
H2 + CuO --> Cu + H2O
_d____d_____d_____d_
nCuO = 3.2 / 80 = 0.04
=> d = 0.04
mHCl = 360 * 18.25 / 100 = 65.7 (g)
nHCl = 65.7 / 36.5 = 1.8 (mol)
=> 8a + 6b + 2c + 2d = 1.8
=> 8a + 6b + 2c + 0.08 = 1.8
=> 8a + 6b + 2c = 1.72
=> 4a + 3b + c = 0.86
a)
theo đlbtkl ta có
mHCl + mhh = mmuối + mH2O + mH2
65.7 + 57.6 = mmuối + 0.86 * 18 + 0.04 * 2
=> mmuối = 107.74 (g)
b) Fe3O4 + 8HCl --> FeCl2 + 2FeCl3 + 4H2O
_a_______8a______a_____2a______4a_
Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
_b______6b_______2b_____3b_
FeO + 2HCl --> FeCl2 + H2O
_b____2b_______b______b_
Fe + 2HCl --> FeCl2 + H2
0.2__0.4_______0.2____0.2
nH2 = nFe = 0.2
232a + 232b =57.6-0.2X56
8a + 8b = 1.8-0.2X2
vô nghiệm vì nFe2O3 =nFeO tuong đương 2ẩn cung M

Theo đề số mol FeO bằng Fe2O3=> Qui đổi hỗn hợp thành Fe3O4
\(n_{Fe_3O_4}=0,01\left(mol\right)\)
\(Fe_3O_4\left(0,01\right)+8HCl\left(0,08\right)\rightarrow FeCl_2+2FeCl_3+4H_2O\)
Theo PTHH: nHCl = 0,08 (mol)
\(\Rightarrow V=\dfrac{0,08}{1}=0,08\left(l\right)\)

Ta có:
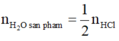
Tương tự bài 1, ta có:
m 5 o x i t + m H C l = m m u o i + m H 2 O s a n p h a m
m
m
u
o
i
=
m
5
o
x
i
t
+
m
H
C
l
-
m
H
2
O
s
a
n
p
h
a
m
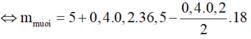
⇔ m m u o i = 7,2g
⇒ Chọn C.

a) \(n_{HCl}=\dfrac{360.18,25\%}{36,5}=1,8\left(mol\right)\)
H2 + CuO ------t°----->Cu + H2O
\(n_{CuO}=\dfrac{43,2}{80}=0,54\left(mol\right)\)
Gọi nCuO phản ứng = x (mol)
Theo đề bài
m chất rắn = \(m_{CuO\left(dư\right)}+m_{Cu}=\left(0,54-x\right).80+x.64=40\)
=> x = 0,2 mol
=> n H2 = 0,2 (mol)
=> m H2 = 0,2 . 2 =0,4 (g)
Fe + 2HCl → FeCl2 + H2 (*)
Theo PT : \(n_{HCl}=2n_{H_2}=0,4\left(mol\right)\)
=> Số mol HCl tác dụng với Fe3O4, Fe2O3, FeO là 1,8 - 0,4 = 1,4 mol
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O (1)
Fe2O3 + 6HCl → 2FeCl3 + 3H2O (2)
FeO + 2HCl → FeCl2 + H2O (3)
Bảo toàn nguyên tố H : \(n_{H_2O}.2=n_{HCl}.1\)
\(\Rightarrow n_{H_2O}=\dfrac{1,4}{2}=0,7\left(mol\right)\)
Áp dụng định luật bảo toàn khối lượng, ta có:
mhỗn hợp + mHCl = mmuối + mH2O + mH2
57,6 + 1,8.36,5 = mmuối + 0,7.18 + 0,4
mmuối= a = 57,6 + 65,7 - 12,6 - 0,4 = 110,3 (gam)
b) Từ PT (*) => \(n_{Fe}=n_{H_2}=0,2\left(mol\right)\)
Nếu trong X, nFe2O3=nFeO
=> Gộp 2 oxit trên thành Fe3O4
Fe3O4 + 8HCl → 2FeCl3 + FeCl2 + 4H2O
\(n_{Fe_3O_4}=\dfrac{57,6-0,2.56}{232}=0,2\left(mol\right)\)
\(n_{FeCl_3}=2n_{Fe_3O_4}=0,4\left(mol\right)\)
\(n_{FeCl_2}=n_{Fe_3O_4}=0,2\left(mol\right)\)
\(m_{ddsaupu}=57,6+360-0,4=417,2\left(g\right)\)
=> \(C\%_{FeCl_3}=\dfrac{0,4.162,5}{417,2}.100=15,58\%\)
\(C\%_{FeCl_2}=\dfrac{0,2.127}{417,2}.100=6,09\%\)

Mình làm câu này rồi nè, bạn tham khảo bài làm của mình ở link này nha
https://hoc24.vn/cau-hoi/hoa-tan-hoan-toan-576-gam-hon-hop-a-gom-fe3o4-fe2o3-feo-fe-trong-dung-dich-hcl-thi-can-dung-360-gam-dung-dich-hcl-1825-de-tac-dung-vua-du-sau-phan-ung-thu-duoc-v-lit-h2-dktc-va-dung-dich-b-c.1336663119282

a) \(n_{HCl}=\dfrac{360.18,25\%}{36,5}=1,8\left(mol\right)\)
Sau phản ứng thu được hỗn hợp rắn gồm Cu và CuO có khối lượng nhỏ hơn khối lượng CuO ban đầu là 3,2 gam.
\(n_{H_2}=n_{O\left(trongCuO\right)}=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Bảo toàn nguyên tố H: \(n_{HCl}=2n_{H_2}+2n_{H_2O}\Rightarrow n_{H_2O}=0,7\left(mol\right)\)
=> \(n_{O\left(trongA\right)}=0,7\left(mol\right)\)
\(m_{muối}=m_{Fe}+m_{Cl}=\left(57,6-0,7.16\right)+1,8.35,5=110,3\left(g\right)\)
b) B gồm FeCl3 và FeCl2
Gọi x,y lần lượt là số mol của FeCl2 và FeCl3
\(\left\{{}\begin{matrix}3x+2y=1,8\\162,5x+127y=110,3\end{matrix}\right.\)
=> \(x=\dfrac{1}{7};y=\dfrac{24}{35}\)
\(m_{ddB}=m_A+m_{ddHCl}-m_{H_2}=417,2\left(g\right)\)
=> \(C\%_{FeCl_3}=\dfrac{\dfrac{1}{7}.162,5}{417,2}.100=5,56\%\)
\(C\%_{FeCl_2}=\dfrac{\dfrac{24}{35}.127}{417,2}.100=20,87\%\)
c) \(n_{HCl\left(bđ\right)}=2.2=4\left(mol\right)\)
Nếu trong X chỉ chứa Fe3O4 thì :
\(n_{HCl}=8n_{Fe_3O_4}=8.\dfrac{100}{232}=3,45\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa Fe2O3 thì :
\(n_{HCl}=6n_{Fe_3O_4}=6.\dfrac{100}{160}=3,75\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa FeO thì :
\(n_{HCl}=2n_{FeO}=2.\dfrac{100}{72}=2,78\left(mol\right)< n_{HCl\left(bđ\right)}\)
Nếu trong X chỉ chứa Fe thì :
\(n_{HCl}=2n_{Fe}=2.\dfrac{100}{56}=3,57\left(mol\right)< n_{HCl\left(bđ\right)}\)
=> HCl luôn dư và X luôn tan hết

a, Ta có: \(n_{CO}=\dfrac{6,72}{22,4}=0,3\left(mol\right)=n_{CO_2}\)
Theo ĐLBT KL, có: mhh + mCO = mFe + mCO2
⇒ mFe = 18,2 + 0,3.28 - 0,3.44 = 13,4 (g)
b, Giả sử: \(\left\{{}\begin{matrix}n_{Ca}=x\left(mol\right)\\n_{Mg}=y\left(mol\right)\end{matrix}\right.\)
⇒ x + y = 0,2 (1)
PT: \(Ca+2HCl\rightarrow CaCl_2+H_2\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(CaCl_2+Na_2CO_3\rightarrow CaCO_{3\downarrow}+2NaCl\)
\(MgCl_2+Na_2CO_3\rightarrow MgCO_{3\downarrow}+2NaCl\)
Theo PT: \(\left\{{}\begin{matrix}n_{CaCO_3}=n_{Ca}=x\left(mol\right)\\n_{MgCO_3}=n_{Mg}=y\left(mol\right)\end{matrix}\right.\)
⇒ 100x + 84y = 18,4 (2)
Từ (1) và (2) ⇒ x = y = 0,1 (mol)
Theo PT: \(\left\{{}\begin{matrix}n_{CaCl_2}=n_{Ca}=0,1\left(mol\right)\\n_{MgCl_2}=n_{Mg}=0,1\left(mol\right)\end{matrix}\right.\)
⇒ a = mCaCl2 + mMgCl2 = 0,1.111 + 0,1.95 = 20,6 (g)
Bạn tham khảo nhé!