Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a. PTHH: \(MnO_2+4HCl\rightarrow MnCl_2+2H_2O+Cl_2\\ 0,9mol:3,6mol\rightarrow0,9mol:1,8mol:0,9mol\)
\(m_{MnO_2}=\dfrac{78,3}{87}=0,9\left(mol\right)\)
\(m_{CtHCl}=3,6.36,5=131,4\left(g\right)\)
\(C\%=\dfrac{m_{Ct}}{m_{Dd}}.100\%\)
\(\Leftrightarrow20\%=\dfrac{131,4}{m_{Dd}}.100\%\)
\(\Leftrightarrow m_{DdHCl}=657\left(g\right)\)
\(V_{Cl_2}=22,4.0,9=20,16\left(l\right)\)
b. \(m_{CtMnCl_2}=0,9.126=113,4\left(g\right)\)
\(m_{dd}=78,3+657-\left(0,9.71\right)=671,4\left(g\right)\)
\(C\%=\dfrac{113,4}{671,4}.100\%=16,89\%\)
c. \(Cl_2+2NaOH\rightarrow H_2O+NaCl+NaClO\\ 0,9mol:1,8mol\rightarrow0,9mol:0,9mol:0,9mol\)
\(CM_{NaOH}=\dfrac{1,8}{0,25}=7,2\)
\(CM_{NaClO}=\dfrac{0,9}{0,25}=3,6\)

\(n_{Mg}=\dfrac{9,6}{24}=0,4\left(mol\right)\)
Pt : \(Mg+2HCl\rightarrow MgCl_2+H_2|\)
1 2 1 1
0,4 0,8 0,4
\(n_{HCl}=\dfrac{0,4.2}{1}=0,8\left(mol\right)\)
\(V_{ddHCl}=\dfrac{0,8}{0,5}=1,6\left(l\right)\)
\(n_{MgCl2}=\dfrac{0,8.1}{2}=0,4\left(mol\right)\)
\(C_{M_{MgCl2}}=\dfrac{0,4}{1,6}=0,25\left(M\right)\)
Chúc bạn học tốt
\(n_{Mg}=\dfrac{9,6}{24}=0,4\left(mol\right)\\ Mg+2HCl\rightarrow MgCl_2+H_2\\ 0,4.......0,8.......0,4......0,4\left(mol\right)\\ V_{ddHCl}=\dfrac{0,8}{0,5}=1,6\left(l\right)\\ V_{ddMgCl_2}=V_{ddHCl}=1,6\left(l\right)\\ \Rightarrow C_{MddMgCl_2}=\dfrac{0,4}{1,6}=0,25\left(M\right)\)

MnO 2 + HCl → MnCl 2 + Cl 2 + 2 H 2 O
Cl 2 + 2NaOH → NaCl + NaClO + H 2 O
n MnO 2 = 0,2 mol; n NaOH = 0,729 mol
Theo phương trình (1) ta có: n Cl 2 = n MnO 2 = 0,2 mol
Theo phương trình (2) ta có: 2 n Cl 2 < n NaOH ⇒ NaOH dư
Dung dịch A gồm: n NaCl = n NaClO = n Cl 2 = 0,2 mol
n NaOH dư = 0,729 – 2.0,2 = 0,329 mol
m dd A = m Cl 2 + m dd NaOH = 0,2.71 + 145,8 = 160g
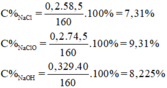

a) CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
b) \(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
CaCO3 + 2HCl --> CaCl2 + CO2 + H2O
_0,1---->0,2------->0,1----->0,1
=> mCaCl2 = 0,1.111 = 11,1 (g)
=> VCO2 = 0,1.22,4 = 2,24 (l)
c) \(a=C_{M\left(HCl\right)}=\dfrac{0,2}{0,4}=0,5M\)
d) \(C_{M\left(CaCl_2\right)}=\dfrac{0,1}{0,4}=0,25M\)

Đáp án C
![]() = 0,8 mol
= 0,8 mol
MnO2 + 4HCl → MnCl2 + Cl2 + 2H2O
0,8 → ![]() = 0,72 (mol)
= 0,72 (mol)
Vkhí = 0,72.22,4 = 16,128 (lit)
nNaOH = 2 (mol)
Cl2 + 2NaOH → NaCl + NaClO + H2O
0,72 2 → 0,72 0,72 (mol)
do NaOH dư, tính theo Cl2
Dung dịch sau phản ứng: nNaCl = nNaClO = 0,72 (mol)
nNaOH dư = 0,56 (mol)
CNaCl = CNaClO = 1,44M, CNaOH = 1,12M

\(a,PTHH:X+2HCl\to XCl_2+H_2\\ \Rightarrow n_{X}=n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ \Rightarrow M_X=\dfrac{9,75}{0,15}=65(g/mol)(Zn)\\ b,n_{HCl}=2.0,2=0,4(mol)\)
Vì \(\dfrac{n_{H_2}}{1}<\dfrac{n_{HCl}}{2}\) nên \(HCl\) dư
\(\Rightarrow n_{ZnCl_2}=n_{H_2}=0,15(mol)\\ \Rightarrow m_{ZnCl_2}=136.0,15=20,4(g)\\ C_{M_{ZnCl_2}}=\dfrac{0,15}{0,2}=0,75M\)

11) Theo đề, ta có: \(n_{MnO_2}=\dfrac{78,3}{87}=0,9\left(mol\right)\)
PTHH: \(MnO_2+4HCl\rightarrow MnCl_2+2H_2O+Cl_2\left(1\right)\)
Số mol: 0,9 mol 3,6 mol 0,9 mol 1,8 mol 0,9 mol
a, Theo phương trình, ta có: \(n_{HCl}=4n_{MnO_2}=4.0,9=3,6\left(mol\right);n_{Cl_2}=n_{MnO_2}=0,9\left(mol\right)\)
\(\Rightarrow m_{HCl}=3,6.36,5=131,4\left(g\right)\)
Mặt khác, C% dung dịch HCl = \(\dfrac{m_{HCl}}{m_{ddHCl}}.100\%\) \(\Leftrightarrow20\%=\dfrac{131,4}{m_{ddHCl}}.100\%\Leftrightarrow m_{ddHCl}=\dfrac{131,4.100}{20}=657\left(g\right)\)(\(m_{ddHCl}\) là khối lượng dung dịch HCl).
\(V_{Cl_2}=0,9.22,4=20,16\left(l\right)\)
b, Theo phương trình, \(n_{MnCl_2}=n_{MnO_2}=0,9\left(mol\right)\)
\(\Rightarrow m_{MnCl_2}=0,9.126=113,4\left(g\right)\)
Mặt khác,
mdung dịch sau phản ứng = \(m_{MnCl_2}+\) mdung dịch HCl - \(m_{Cl_2}\)
= \(78,3+657-\left(0,9.35,5.2\right)\)
= 671,4 (g)
\(\Rightarrow C\%\)dung dịch \(MnCl_2\) = \(\dfrac{113,4}{671,4}.100\%=16,89\%\)
c, Theo (1), \(n_{Cl_2}=n_{MnCl_2}=0,9\left(mol\right)\)
PTHH: \(Fe+\dfrac{3}{2}Cl_2\rightarrow FeCl_3\left(2\right)\)
Số mol: 0,6 \(\rightarrow\) 0,9 \(\rightarrow\) 0,6
Theo (2) \(\Rightarrow n_{FeCl_3}=n_{Fe}=0,6\left(mol\right)\)
\(\Rightarrow m_{FeCl_3}=0.6.162,5=97,5\left(g\right)\)
\(\Rightarrow m\) dung dịch muối thu được = 97,5 + 52,5 =150 (g).
\(\Rightarrow C\%\)dung dịch \(FeCl_3\)= \(\dfrac{97,5}{150}.100\%=65\%\)