Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{1,12}{22,4}=0,05(mol)\\ Fe+2HCl\to FeCl_2+H_2\\ \Rightarrow n_{Fe}=0,05(mol)\\ \Rightarrow \%_{Fe}=\dfrac{0,05.56}{20}.100\%=14\%\\ \Rightarrow \%_{Cu}=100\%-14\%=86\%\)

2Al + 6HCl → 2 A l C l 3 + 3 H 2
a……….3/2.a (mol)
Mg + 2HCl → M g C l 2 + H 2
b....................b (mol)
4 gam rắn không tan là Cu, gọi số mol của Al và Mg lần lượt là a và b (mol). Ta có:
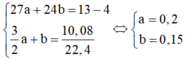
⇒ % m C u = 4 13 .100 = 30,77 % ⇒ % m A l = 0,2.27 13 .100 = 41,54 % ⇒ % m M g = 100 % − 30,77 % − 41,54 % = 27,69 %
⇒ Chọn C.

Phần 1
2Al +6 HCl ----> 2AlCl3 + 3H2 (1)
Fe + 2HCl ----> FeCl2 + H2 (2)
Cu ko pư với dd HCl
Phần 2
2Al + 2NaOH + 2H20 ---> 2NaAlO2 + 3H2 (3)
Fe và Cu ko pư với dd NaOH
Theo pt(3) n Al = \(\frac{2}{3}\).n H2=\(\frac{2}{3}\). \(\frac{3,36}{22,4}\)=0,1 (mol)
%m Al= \(\frac{0,1.27}{20}\).100%= 13,5%
Theo pt(1)(2) tổng n H2=\(\frac{3}{2}\). nAl + n Fe=\(\frac{5,6}{22,4}\)
==> 0,15 + n Fe = 0,25 ==> n Fe = 0,1 (mol)
%m Fe= \(\frac{0,1.56}{20}\).100%= 28%
%m Cu=100% - 13,5% - 28% =58,5%
tại sao % Al lại đem chia 20 vậy 0,1 mol là ở 1 phần thôi là chia 10 chứ .% Fe cũng thế vậy
==> tổng mAl + mFe trong 1 phần = 0,1.27 + 0,1.56=8,3
%Cu =100% - \(\dfrac{8,3}{10}\).100=17%

\(n_{H_2}=\dfrac{7,437}{24,79}=0,3(mol)\\ PTHH:2Al+6HCl\to 2AlCl_3+3H_2\\ \Rightarrow n_{Al}=\dfrac{2}{3}n_{H_2}=0,2(mol)\\ \Rightarrow m_{Al}=0,2.27=5,4(g)\\ \Rightarrow m_{Cu}=m_{hh}-m_{Al}=10-5,4=4,6(g)\)

Gọi số mol của Al và Fe lần lượt là a và b
Ta có 1,5a + b = 0,25
1,5a = 0,15
=> a = 0,1 và b = 0,1
=> %Al = 32,53%
%Fe= 67,47%

Cu không tác dụng với axit HCl , do đó chất không tan là Cu và m Cu = 2,5 (gam).
Khối lượng Al và Mg bằng : 12,7 - 2,5 = 10,2 (gam)
Phương trình hoá học của phản ứng :
2Al + 6HCl → 2 AlCl 3 + 3 H 2
Mg + 2HCl → MgCl 2 + H 2
Theo phương trình hoá học trên và dữ kiện đề bài cho, ta có :
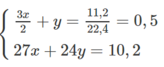
Giải ra, ta có : x = y = 0,2 mol
m Al = 0,2 x 27 = 5,4g
m Mg = 0,2 x 24 = 4,8g
% m Al = 5,4/12,7 .100% = 42,52%
% m Mg = 4,8/12,7 .100% = 37,8%
% m Cu = 100% - 42,52% - 37,8% = 19,68%

Gọi số mol Fe, Al là a,b
Khối lượng kim loại không tan là khối lượng của Cu
=> 56a + 27b = 9,08-2,4 = 6,68(g)
\(n_{H_2}=\dfrac{3,584}{22,4}=0,16\left(mol\right)\)
PTHH: Fe + 2HCl --> FeCl2 + H2
______a------------------------>a
2Al + 6HCl --> 2AlCl3 + 3H2
_b------------------------->1,5b
=>a + 1,5b = 0,16 (mol)
=> a = 0,1; b = 0,04
=> mFe = 0,1.56 = 5,6 (g)
=> mAl = 0,04.27 = 1,08(g)
do Cu không tác dụng với HCL , AL thì tác dụng với HCL
nên ta có AL +3HCL \(\rightarrow\)ALCL3 +\(\frac{3}{2}\)H2
số mol của khí =0,15
=>số mol của AL =\(0.15\div\frac{3}{2}\)
phần trăm của AL= \(\frac{\left(0.15\div\frac{3}{2}\right)\times27}{5}\times100\)=54%
n H2 = 3,36/ 22,4 =0,15 mol
vì cho hỗn hợp vào dung dịch HCl dư thì Cu ko t/ d nên khí H2 thoát ra là của Al phản ứng :
pthh: 2Al + 6HCl ---> 2AlCl3 + 3H2
theo pthh n Al = 2/3 n H2 = 2/3. 0,15 = 0,1 mol
---> %m Al=((0,1 .27)/5) . 100 =54%