Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình phản ứng:
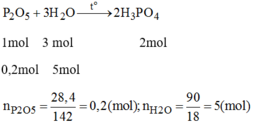
Tỉ lệ mol:
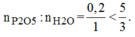
Vậy H 2 O dư và P 2 O 5 hết.
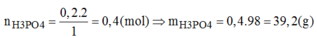
→ Chọn C.

+ta có:
2P + 5/2O2====> P205
0,2 0,3125 0,1
Xét tỉ lệ:
===> oxi dư. và n02 dư=0,025( mol)==> mo2 dư= 0,8(g)
b, mP205= 0,1.( 31.2+ 16.5)=14,2g
c, P205+ 3H20------> 2H3PO4
0,1 0,2
===> KHỐI LƯỢNG H3P04 là: 19,6

nAl = 0,5 mol
nO2 = 0,3 mol
4Al + 3O2 \(\underrightarrow{t^o}\) 2Al2O3
Đặt tỉ lệ ta có
\(\dfrac{0,5}{4}\) > \(\dfrac{0,3}{3}\)
\(\Rightarrow\) Al dư
\(\Rightarrow\) mAl dư = ( 0,5 - 0,4 ).27 = 2,7 (g)
\(\Rightarrow\) mAl2O3 = 0,2.102 = 20,4 (g)

\(n_P=\dfrac{6,2}{31}=0,2mol\)
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(4P+5O_2\rightarrow\left(t^o\right)2P_2O_5\)
Xét: \(\dfrac{0,2}{4}\) < \(\dfrac{0,3}{5}\) ( mol )
0,2 0,1 ( mol )
\(m_{P_2O_5}=0,1.142=14,2g\)
`PTHH: 4P + 5O_2` $\xrightarrow[]{t^o}$ `2P_2 O_5`
`n_P = [ 6,2 ] / 31 = 0,2 (mol)`
`n_[O_2] = [ 6,72 ] / [ 22,4 ] = 0,3 (mol)`
Ta có: `[ 0,2 ] / 4 < [ 0,3 ] / 5`
`->P` hết ; `O_2` dư
Theo `PTHH` có: `n_[P_2 O_5] = 1 / 2 n_P = 1 / 2 . 0,2 = 0,1 (mol)`
`-> m_[P_2 O_5] = 0,1 . 142 = 14,2 (g)`

PTHH:P2O5+3H2O\(\underrightarrow{t^0}\)2H3PO4
Theo PTHH:142 gam P2O5 cần 54 gam H2O
Vậy:7,1 gam P2O5 cần 2,7 gam H2O
Do đó:P2O5 thừa:28,4-7,1=21,3(gam)
Vì P2O5 thừa nên ta tính SP theo chất thiếu là:H2O
Theo PTHH:54 gam H2O tạo ra 196 gam H3PO4
Vậy:2,7 gam H2O tạo ra 9,8 gam H3PO4
Vậy mH3PO4=9,8 gam
Ta có: \(n_{P_2O_5}=\frac{28,4}{142}=0,2\left(mol\right)\\ n_{H_2O}=\frac{2,7}{18}=0,15\left(mol\right)\)
PTHH: P2O5 + 3H2O -to-> 2H3PO4
Theo PTHH và đề bài, ta có:
\(\frac{0,2}{1}>\frac{0,15}{3}\)
=> P2O5 dư, H2O hết nên tính theo \(n_{H_2O}\)
Theo PTHH và đề bài, ta có:
\(n_{H_3PO_4}=\frac{2.0,15}{3}=0,1\left(mol\right)\)
Khối lượng H3PO4 tạo thành sau phản ứng:
\(m_{H_3PO_4}=0,1.98=9,8\left(g\right)\)

a) P2O5 + 3H2O --> 2H3PO4
b) \(n_{H_2O}=\dfrac{45}{18}=2,5\left(mol\right)\)
\(n_{P_2O_5}=\dfrac{14,2}{142}=0,1\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{2,5}{3}>\dfrac{0,1}{1}\) => P2O5 hết, H2O dư
PTHH: P2O5 + 3H2O --> 2H3PO4
0,1---->0,3------>0,2
=> \(m_{H_2O\left(dư\right)}=\left(2,5-0,3\right).18=39,6\left(g\right)\)
c) \(m_{H_3PO_4}=0,2.98=19,6\left(g\right)\)

a)
\(4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)
b)
Ta thấy :
\(\dfrac{n_P}{4} = \dfrac{\dfrac{12,4}{31}}{4} =0,1 < \dfrac{n_{O_2}}{5} = \dfrac{\dfrac{20}{32}}{5} = 0,125\)
do đó, O2 dư
\(n_{O_2\ pư} = \dfrac{5}{4}n_P = 0,5(mol)\\ \Rightarrow n_{O_2\ dư} = \dfrac{20}{32} - 0,5 = 0,125(mol)\)
c)
\(n_{P_2O_5} = \dfrac{1}{2}n_P = 0,2(mol)\\ \Rightarrow m_{P_2O_5} =0,2.142 = 28,4(gam)\)


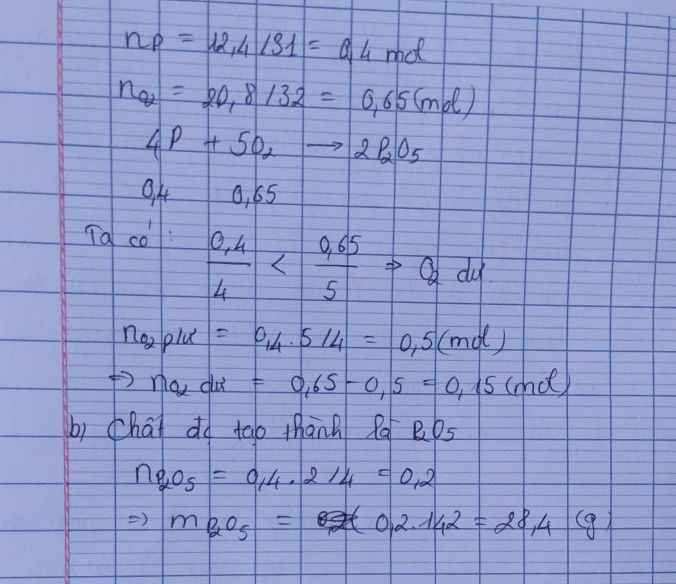
PT: \(P_2O_5+3H_2O\rightarrow2H_3PO_4\)
Số mol P2O5 tham gia phản ứng là: \(n_{P_2O_5}=\dfrac{28,4}{142}=0,2\left(mol\right)\)
Số mol H2O tham gia phản ứng là: \(n_{H_2O}=\dfrac{90}{18}=5\left(mol\right)\)
Ta có tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{5}{3}\) => H2O dư
Theo phương trình,ta có: \(n_{H_3PO_4}=2.n_{P_2O_5}=2.0,2=0,4\left(mol\right)\)
=> Khối lượng H3PO4 tạo thành là:
\(m_{H_3PO_4}=0,4.98=39,2\left(g\right)\)
=.= hk tốt!!
\(n_{P_2O_5}=\dfrac{28,4}{142}=0,2\left(mol\right)\)
\(n_{H_2O}=\dfrac{90}{18}=5\left(mol\right)\)
PTHH: \(P_2O_5+3H_2O->2H_3PO_4\)
Theo PTHH ta có tỉ lệ:
\(\dfrac{0,2}{1}< \dfrac{5}{3}=>\) \(H_2O\) dư. \(P_2O_5\) hết => tính theo \(n_{P_2O_5}\)
Theo PT ta có: \(n_{H_3PO_4}=\dfrac{0,2.2}{1}0,4\left(mol\right)\)
=> \(m_{H_3PO_4}=0,4.98=39,2\left(g\right)\)