Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

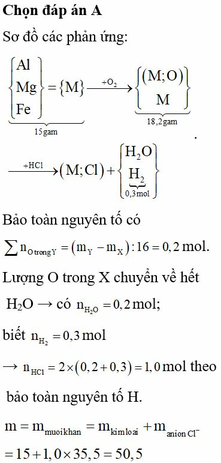
Chọn đáp án A
+ BTKL có nO/oxit = (18,2 – 15) ÷ 16 = 0,2 mol || nH2 = 0,3 mol
⇒ ∑nHCl đã pứ = 2nO/oxit + 2nH2 = 1 mol ⇒ mCl–/muối = 35,5 gam
⇒ mmuối = mkim loại + mCl–/muối = 15 + 35,5 = 50,5 gam ⇒ Chọn A

Đáp án D
![]()
=> nHCl = 2nO + nH2 = 2.0,2 + 2.0,3 = 1 mol
m = 15 + 1.35,5 = 50,5

\(Al+NaOH+H_2O\underrightarrow{t^o}NaAlO_2+\dfrac{3}{2}H_2\)
0.2 <--- 0.3
Fe không phản ứng với dung dịch NaOH
\(n_{H_2}=\dfrac{6.72}{22.4}=0.3mol\)
\(\%m_{Al}=\dfrac{0.2\times27\times100}{15}=36\%\)
\(\%m_{Fe}=100-36=64\%\)
Al+NaOH+H2Oto→NaAlO2+32H2Al+NaOH+H2Oto→NaAlO2+32H2
0.2 <--- 0.3
Fe không phản ứng với dung dịch NaOH
nH2=6.7222.4=0.3molnH2=6.7222.4=0.3mol
%mAl=0.2×27×10015=36%%mAl=0.2×27×10015=36%
%mFe=100−36=64%%mFe=100−36=64%
(Chắc thế)

Đặt nO = z mol
TN1: ne (1) = 2z + 8nN2O + 3nNO + 8nNH4+ => ne (1) = 2z + 8.0,04 + 3.0,26 + 8nNH4+
TN2: ne (2) = 2z + 2nSO2 => ne (2) = 2z + 2.0,7
Mà ne(1) = ne(2) => nNH4+ = 0,0375 (mol)
TN1: nNO3-(muối KL) = ne = 2z + 1,4 (mol)
m muối (1) = mKL + mNO3-(muối KL) + mNH4NO3 => mKL + 62(2z + 1,4) + 80.0,0375 = 129,4 (1)
TN2: mSO42- = ne/2 = z + 0,7
m muối (2) = mKL + mSO42- => mKL + 96(z + 0,7) = 104 (2)
Từ (1) và (2) => mKL = 27,2 gam và z = 0,1 mol
=> m = mKL + mO = 27,2 + 0,1. 16 = 28,8 gam
Đáp án B

Đáp án C
Các phản ứng xảy ra:
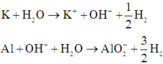
Vì hai trường hợp có khối lượng hỗn hợp đem hòa tanlà như nhau mà thể tích H2 thu được khác nhau nên khihòa tan hỗn hợp vào nước, một phần Al dư đã khôngtan. Gọi nK = a; nAl = n có:
+ Khi hòa tan vào nưóc dư: ![]()
+ Khi hòa tan vào dd NaOH dư: ![]()
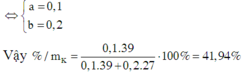
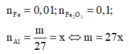
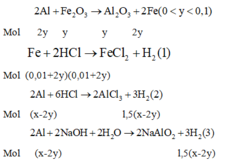

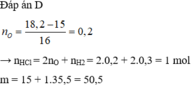
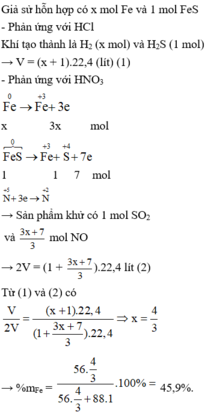
Đáp án C