Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Phương trình hóa học của các phản ứng:
H2 + CuO → Cu + H2O (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b) Trong phản ứng (1), (2) chất khử H2 vì chiếm oxi của chất khác, chất oxi hóa là CuO và Fe2O3 vì nhường oxi cho chất khác.
c) Khối lượng đồng thu được từ 6g hỗn hợp 2 kim loại thu được:
mCu = 6g - 2,8g = 3,2g, nCu = 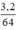 = 0,05 mol
= 0,05 mol
nFe = 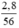 = 0,05 (mol)
= 0,05 (mol)
nH2 (1) = nCu = 0,05 mol ⇒ VH2(1) = 22,4 . 0,05 = 1,12 lít
nH2 (2) = 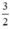 . nFe =
. nFe = 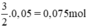 ⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
⇒ VH2 (2) = 22,4 . 0,075 = 1,68 lít khí H2.
VH2 = VH2(1) + VH2(2) = 1,12 + 1,68 = 2,8(l)

a)\(CH_4+2O_2\underrightarrow{t^o}CO_2+2H_2O\)
\(C+O_2\underrightarrow{t^o}CO_2\)
\(S+O_2\underrightarrow{t^o}SO_2\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
b)\(Fe_2O_3+3H_2\rightarrow2Fe+3H_2O\)
\(HgO+H_2\rightarrow Hg+H_2O\)
\(PbO+H_2\rightarrow Pb+H_2O\)
c)\(2Na+2H_2O\rightarrow2NaOH+H_2\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(Na_2O+H_2O\rightarrow2NaOH\)
\(SO_2+H_2O\rightarrow H_2SO_3\)
\(P_2O_5+3H_2O\rightarrow2H_3PO_4\)

a)
cho que đóm đang cháy vào 3 lọ khí
cháy mãnh liệt hơn => Oxi
cháy với ngọn lửa màu xanh => Hidro
cháy bình thường => Không khí
b)
CO2 - cacbon đioxit
Fe3O4 - sắt từ oxit
CaO - canxi oxit
SO3 - lưu huỳnh trioxit
CO2 là tên thường gọi thôi, phải gọi đầy đủ là "khí cacbonic" và chuẩn hơn là cacbon đioxit

1)
Trích mẫu thử
Sục mẫu thử vào dung dịch nước vôi trong :
- mẫu thử tạo vẩn đục trắng là $CO_2$
$CO_2 + Ca(OH)_2 \to CaCO_3 + H_2O$
Nung nóng mẫu thử còn với Cu :
- mẫu thử làm chất chuyển từ màu nâu đỏ sang đen là $O_2$
$2Cu + O_2 \xrightarrow{t^o} 2CuO$
- mẫu thử không hiện tượng là $N_2$
Câu 2 :
Oxit là $CuO,SO_2,CO_2$
Câu 3 :
- Oxit bazo :
$Fe_2O_3$ : Sắt III oxit
$ZnO $: Kẽm oxit
$K_2O$ : Kali oxit
- Oxit axit :
$CO_2 $ : Cacbon đioxit
$SO_2$ : Lưu huỳnh đioxit
$P_2O_3$ : Điphotpho trioxit
$N_2O_5$ : Đinito pentaoxit
- Oxit trung tính :
$CO$ : Cacbon monooxit

nZn = 6,5 : 65 = 0,1 (mol)
nH2SO4 = 14,7 : 98 = 0,15 (mol)
pthh : Zn + 2HCl --> ZnCl2 + H2
LTL :
0,1/1 < 0,15/2 => Zn dư
theo pthh , nH2SO4 = 1/2 nH2 = = 0,075 (mol)
=>VH2 = 0,075 . 22,4 = 1,68 (l)
13.
Chất tác dụng với nước ở nhiệt độ thường là:K,CaO,SO3
\(2K+2H_2O\rightarrow2KOH+H_2\)
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\)
\(SO_3+H_2O\rightarrow H_2SO_4\)
14.
Dẫn các khí qua dd \(Ca\left(OH\right)_2\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\) ( kết tủa trắng )
-H2,O2: không hiện tượng
Đưa que đóm đang cháy vào 2 khí còn lại:
-O2: cháy bùng lên
-H2:cháy với ngọn lửa xanh, nổ nhẹ
15.\(n_{Zn}=\dfrac{6,5}{65}=0,1mol\)
\(n_{H_2SO_4}=\dfrac{14,7}{98}=0,15mol\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
0,1 < 0,15 ( mol )
0,1 0,1 ( mol )
\(V_{H_2}=0,1.22,4=2,24l\)

CuO+H2-t0-> Cu +H2O
Fe2O3+3H2-t0->2Fe+3H2O
chất khử là H2
chất oxi hóa là CuO và Fe2O3. vì chất khử là chất chiếm oxi của chất khác, còn chất oxi hóa là chất nhường oxi cho chất khác
theo đề bài ->mFe=2,8 g->nFe=0,05 mol
=>mCu=6-2,8=3,2 g->nCu=0,05mol
theo PTPỨ =>nCu=nH2=0,05 mol
3nH2=2nFe->nH2=(2/3)*0,05=1/30 mol
do đó VH2 phản ứng là: (0,05+1/30)*22,4=1,867 lít
câu 2
a)Zn+H2SO4->ZnSO4+H2
2Al+3H2SO4->Al2(SO4)3+3H2
Fe+H2SO4->FeSO4+H2
b) Fe
cậu chỉ cần đặt a là số gam của từng kim loai.(vì khối lượng của mỗi kim loại bằng nhau). Sau đó theo phương trình cậu tính khối lượng khí H2 ở mỗi phương trình rồi so sánh là được
c) Fe cách tính gần giống phần b nên tự logic nha

a) PTHH:
CuO + H2 =(nhiệt)=> Cu + H2O (1)
Fe2O3 + 3H2 =(nhiệt)=> 2Fe + 3H2O (2)
b) - Dựa vào định nghĩa chất khử và chất oxi hóa
=> Chất khử: H2
Chất Oxi hóa: CuO và Fe2O3
c) Lượng đồng có trong 6g hỗn hợp 2 kim loại thu được:mCu = 6g - 2,8g = 3,2g.
VH2 cần dùng theo phương trình phản ứng(1) = \(\dfrac{3,2}{64}\cdot64=1,12\left(l\right)\) =
VH2 cần dùng theo phương trình phản ứng(2) = \(\dfrac{2,8}{56}\cdot\dfrac{3}{2}\cdot22,4=1,68\left(l\right)\)
a.Phương trình phản ứng:
CuO + H2 Cu + H2O (1)
1mol 1mol 1mol 1mol
Fe2O3 + 3H2 3H2O + 2Fe (2)
1mol 3mol 3mol 2mol
b. + Chất khử là H2 vì chiếm oxi của chất khác;
+ Chất oxi hóa: CuO, Fe2O3 vì nhường oxi cho chất khác.
c. Số mol đồng thu được là: nCu = = 0,5 (mol)
Số mol sắt là: nFe = = 0,05 (mol)
Thể tích khí H2 cần dùng để khử CuO theo phương trình phản ứng (1) là: nH2 = nCu = 0,05 mol => VH2 = 22,4.0,05 = 1,12 (lít)
Khí H2 cần dùng để khử Fe2O3 theo phương trình phản ứng (2) là:
nH2 = nFe =
.0,05 = 0,075 mol
=>VH2(đktc) = 22,4.0,075 = 1,68 (lít)
1/ a/ Lấy mẫu thử và đánh dấu từng mẫu thử
Cho quỳ tím vào các mẫu thử
Hóa đỏ: H2SO4. Hóa xanh: KOH. quỳ tím không đổi màu là nước
b/ Lấy mẫu thử và đánh dấu từng mẫu thử
Cho các mẫu thử vào nước
Tan: K2O, CaO. Không tan: MgO
K2O + H2O => 2KOH
CaO + H2O => Ca(OH)2
Cho H2SO4 vào các mẫu thử tan trong nước, xuất hiện kết tủa trắng là Ca(OH)2
Ca(OH)2 + H2SO4 => CaSO4 + 2H2O
c/ Lấy mẫu thử và đánh dấu từng mẫu thử
Cho que đóm vào các mẫu thử
Que đóm cháy bình thường là không khí
Que đóm cháy sáng => O2
Que đóm cháy với ngọn lửa màu xanh và kèm tiếng nổ nhỏ => H2
2/ CO2 + H2O => (pứ hai chiều) H2CO3:axit yếu
Na + H2O => NaOH + 1/2 H2
CaO + H2O => Ca(OH)2
K + H2O => KOH + 1/2 H2
P2O5 + 3H2O => 2H3PO4
3/ Điều chế oxi trong PTN dùng: KMnO4 và KClO3
2KMnO4 => K2MnO4 + MnO2 + O2
2KClO3 => 2KCl + 3O2
Nếu số mol hai lượng chất bằng nhau
Theo phương trình: => V1/V2 = 1/3