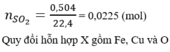Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(a) 2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O\)(Phản ứng oxi hóa-khử)
\(Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O\)
\(b) n_{SO_2} = \dfrac{672}{1000.22,4} = 0,03(mol)\\ n_{Fe}= \dfrac{2}{3}n_{SO_2} = 0,02(mol)\\ \%m_{Fe} = \dfrac{0,02.56}{2,72}.100\% = 41,18\%\\ \%m_{Fe_2O_3} = 100\% -41,18\% = 58,82\%\)

a)
$FeO + 2HCl \to FeCl_2 + H_2O$
$Fe + 2HCl \to FeCl_2 + H_2$
$2FeO + 4H_2SO_4 \to Fe_2(SO_4)_3 + SO_2 + 4H_2O$
$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
b)
n Fe = n H2 = 4,48/22,4 = 0,2(mol)
n SO2 = 7,84/22,4 = 0,35(mol)
Bảo toàn e :
n FeO + 3n Fe = 2n SO2
=> n FeO = 0,35.2 - 0,2.3 = 0,1(mol)
=> m = 0,1.72 + 0,2.56 = 18,4 gam

a.b.
\(n_{Al}=\dfrac{4,05}{27}=0,15mol\)
\(2Al+6H_2SO_4\left(đ\right)\rightarrow\left(t^o\right)Al_2\left(SO_4\right)_3+3SO_2+6H_2O\)
0,15 0,225 ( mol )
\(V_{SO_2}=0,225.22,4=5,04l\)
c.
\(Ba\left(OH\right)_2+SO_2\rightarrow BaSO_3+H_2O\)
\(Ba\left(OH\right)_2+2SO_2\rightarrow Ba\left(HSO_3\right)_2\)
Gọi \(\left\{{}\begin{matrix}n_{BaSO_3}=x\\n_{Ba\left(HSO_3\right)_2}=y\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}217x+299y=38,7\\x+2y=0,225\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,075\\y=0,075\end{matrix}\right.\)
\(n_{Ba\left(OH\right)_2}=0,075+0,075=0,15mol\)
\(V_{Ba\left(OH\right)_2}=\dfrac{0,15}{1}=0,15l\)
a.b.
nAl=4,0527=0,15molnAl=4,0527=0,15mol
2Al+6H2SO4(đ)→(to)Al2(SO4)3+3SO2+6H2O2Al+6H2SO4(đ)→(to)Al2(SO4)3+3SO2+6H2O
0,15 0,225 ( mol )
VSO2=0,225.22,4=5,04lVSO2=0,225.22,4=5,04l
c.
Ba(OH)2+SO2→BaSO3+H2OBa(OH)2+SO2→BaSO3+H2O
Ba(OH)2+2SO2→Ba(HSO3)2Ba(OH)2+2SO2→Ba(HSO3)2
Gọi {nBaSO3=xnBa(HSO3)2=y{nBaSO3=xnBa(HSO3)2=y
→{217x+299y=38,7x+2y=0,225→{217x+299y=38,7x+2y=0,225 ⇔{x=0,075y=0,075⇔{x=0,075y=0,075
nBa(OH)2=0,075+0,075=0,15molnBa(OH)2=0,075+0,075=0,15mol
VBa(OH)2=0,151=0,15l

Bài 1 :
\(NaCl + H_2SO_{4_{đặc}} \xrightarrow{t^o} NaHSO_4 + HCl\\ MnO_2 + 4HCl \to MnCl_2 + Cl_2 + 2H_2O\\ Cl_2 + SO_2 + 2H_2O \to 2HCl + H_2SO_4\\ Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + 2H_2O\)

Câu 2:
\(n_{Cl_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ PTHH:2Fe+3Cl_2\xrightarrow{t^o} 2FeCl_3\\ \Rightarrow n_{Fe}=0,2(mol)\\ \Rightarrow m=m_{Fe}=0,2.56=11,2(g)\)
Câu 3:
Đặt \(\begin{cases} n_{Fe}=x(mol)\\ n_{Mg}=y(mol) \end{cases} \)
\(a,n_{H_2}=\dfrac{5,6}{22,4}=0,25(mol) PTHH:Fe+2HCl\to FeCl_2+H_2\\ Mg+2HCl\to MgCl_2+H_2\\ \Rightarrow \begin{cases} 56x+24y=10,16\\ x+y=0,25 \end{cases} \Rightarrow\begin{cases} x=0,13(mol)\\ y=0,12(mol) \end{cases}\\ \Rightarrow \begin{cases} \%_{Fe}=\dfrac{0,13.56}{10,16}.100\%=71,65\%\\ \%_{Mg}=100\%-71,65\%=28,35\% \end{cases}\\ b,\Sigma n_{HCl}=2n_{Fe}+2n_{Mg}=0,5(mol)\\ \Rightarrow C_{M_{HCl}}=\dfrac{0,5}{0,5}=1M\)

Ta có: \(n_{SO_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
\(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
Coi hh chất rắn gồm M và O.
⇒ nO = 0,15.2 = 0,3 (mol)
Ta có: \(n_M=\dfrac{16,2}{M_M}\left(mol\right)\)
BT e, có: n.nM = 2nO + 2nSO2 + 6nS
\(\Rightarrow\dfrac{16,2n}{M_M}=1,8\Rightarrow M_M=9n\left(g/mol\right)\)
Với n = 3 thì MM = 27 (g/mol) là thỏa mãn.
Vậy: M là Al.