Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 2Al + 3Cl2 --to--> 2AlCl3
b) \(n_{AlCl_3}=\dfrac{13,35}{133,5}=0,1\left(mol\right)\)
PTHH: 2Al + 3Cl2 --to--> 2AlCl3
0,1<-0,15<---------0,1
=> VCl2 = 0,15.22,4 = 3,36(l)
c) mAl = 0,1.27 = 2,7(g)
\(a.PTHH:2Al+3Cl_2\overset{t^o}{--->}2AlCl_3\)
b. Ta có: \(n_{AlCl_3}=\dfrac{13,35}{133,5}=0,1\left(mol\right)\)
Theo PT: \(n_{Cl_2}=\dfrac{3}{2}.n_{AlCl_3}=\dfrac{3}{2}.0,1=0,15\left(mol\right)\)
\(\Rightarrow V_{Cl_2}=0,15.22,4=3,36\left(lít\right)\)
c. Theo PT: \(n_{Al}=n_{AlCl_3}=0,1\left(mol\right)\)
\(\Rightarrow m_{Al}=0,1.27=2,7\left(g\right)\)

m C l = m A l C l 3 - m A l = 6,675 - 1,35 = 5,325 g
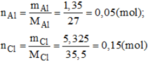
n C l = 3 . n A l ⇒ số nguyên tử Cl gấp 3 số nguyên tử Al. Công thức hóa học đơn giản của nhôm clorua: A l C l 3

\(n_{Al}=\frac{1,08}{27}=0,04mol\)
\(2Al+3Cl_2\rightarrow^{t^o}2AlCl_3\)
a) \(n_{Cl_2}=\frac{3}{2}.0,04=0,06mol\)
\(V_{Cl_2}=0,06.22,4=1,344l\)
b) Cách 1: \(m_{AlCl_3}=m_{Al}+m_{Cl_2}=1,08+71.0,06=5,34g\)
Cách 2: \(n_{AlCl_3}=n_{Al}=0,04mol\)
\(m_{AlCl_3}=0,04.133,5=5,34g\)

Câu 1)
a) 2HgO\(-t^0\rightarrow2Hg+O_2\)
b)Theo gt: \(n_{HgO}=\frac{2,17}{96}\approx0,023\left(mol\right)\\ \)
theo PTHH : \(n_{O2}=\frac{1}{2}n_{HgO}=\frac{1}{2}\cdot0,023=0,0115\left(mol\right)\\ \Rightarrow m_{O2}=0,0115\cdot32=0,368\left(g\right)\)
c)theo gt:\(n_{HgO}=0,5\left(mol\right)\)
theo PTHH : \(n_{Hg}=n_{HgO}=0,5\left(mol\right)\\ \Rightarrow m_{Hg}=0,5\cdot80=40\left(g\right)\)
Câu 2)
a)PTHH : \(S+O_2-t^0\rightarrow SO_2\)
b)theo gt: \(n_{SO2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
theo PTHH \(n_S=n_{SO2}=0,1\left(mol\right)\\ \Rightarrow m_S=0,1\cdot32=3,2\left(g\right)\)
Ta có khối lượng S tham gia là 3,25 g , khối lượng S phản ứng là 3,2 g
Độ tinh khiết của mẫu lưu huỳnh là \(\frac{3,2}{3,25}\cdot100\%\approx98,4\%\)
c)the PTHH \(n_{O2}=n_{SO2}=0,1\left(mol\right)\Rightarrow m_{O2}=0,1\cdot32=3,2\left(g\right)\)

a) $2Al + 3Cl_2 \xrightarrow{t^o} 2AlCl_3$
b) $n_{Al} = \dfrac{5,4}{27} = 0,2(mol)$
Theo PTHH : $n_{Cl_2} = \dfrac{3}{2}n_{Al} = 0,3(mol)$
$\Rightarrow V_{Cl_2} = 0,3.24,79 = 7,437(lít)$
c) $n_{AlCl_3} = n_{Al} = 0,2(mol)$
$\Rightarrow m_{AlCl_3} = 0,2.133,5 = 26,7(gam)$

\(n_{Al}=\dfrac{1,08}{27}=0,04\left(mol\right)\\ 2Al+3Cl_2\rightarrow\left(t^o\right)2AlCl_3\\ a,n_{Cl_2}=\dfrac{3}{2}.0,04=0,06\left(mol\right)\\ V_{Cl_2\left(\text{Đ}KTC\right)}=0,06.22,4=1,344\left(l\right)\\ b,C1:m_{AlCl_3}=m_{Al}+m_{Cl_2}=1,08+71.0,06=5,34\left(g\right)\\ C2:n_{AlCl_3}=n_{Al}=0,04\left(mol\right)\\ m_{AlCl_3}=0,04.133,5=5,34\left(g\right)\)
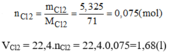
Bài 1 : mFe ko thể tính bằng 2 cách được , chỉ có mFe3O4 mới tính được
Theo đề bài ta có :
nO2 = \(\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Ta có PTHH :
\(3Fe+2O2-^{t0}->Fe3O4\)
0,3mol...0,2mol..............0,1mol
Ta có :
mFe = 0,3.56 = 16,8 (g)
Cách 1 :
mFe3O4 = 0,1 . 232 = 23,2(g)
Cách 2 :
Áp dụng ĐLBTKL ta có :
mFe + mO2 = mFe3O4
=> mFe3O4 = 56.0,3 + 0,2.32 = 23,2(g)
Vậy.......
Bài 2 : Theo đề bài ta có : nAl = \(\dfrac{2,7}{27}=0,1\left(mol\right)\)
a) CTHH của nhôm là Al
CTHH của khí clo là Cl2
=> CTHH đơn giản của nhôm lorua là : \(Al_xCl_y\)
Ta có PTHH :
\(2xAl+yCl2-^{t0}->2Al_xCl_y\)
\(0,1mol......\dfrac{0,1.y}{2x}mol\)
Ta có :
\(mAlxCly=mAl+mCl=>mCl=13,35-2,7=10,65\left(g\right)\)
=> nCl = \(\dfrac{10,65}{35,5}=0,3\left(mol\right)\)
Ta có :
x : y = nAl : nCl = 0,1 : 0,3 = 1 : 3
=> CTHH của nhôm clorua là AlCl3
b) Ta có : nCl2 = \(\dfrac{0,1y}{2x}nAl=\dfrac{0,1.3}{2}=0,15\left(mol\right)\)
Thể tích khí clo đã tham gia là : VCl2(đktc) = 0,15.22,4 = 3,36 (l)
Vậy............