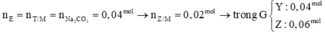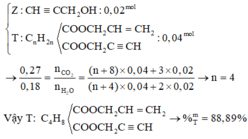Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Chọn B.
Khi đốt cháy A ta có:
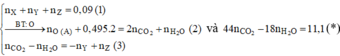
Khi cho A tác dụng với KOH thì:
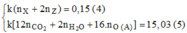
Lấy (1) + (3) ta được: nX + 2nZ = + 0,09 rồi thay vào (4): k( + 0,09) = 0,15
Lập tỉ lệ:
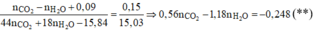
Từ (*) và (**) suy ra: n C O 2 = 0 , 42 m o l ; n H 2 O = 0 , 41 m o l ⇒ m A = 10 , 02 g a m
Tiếp tục giải hệ đốt cháy tìm được: nX = 0,02; nY = 0,03; nZ = 0,04.
Trong 15,03 gam A thì: → B T K L m = 16,38 (g).

Chọn đáp án C
“Giả thiết chữ”: ancol hai chức là C3H6(OH)2 và cũng chính là ancol tạo este.
→ Axit tạo este cùng với axit trong hỗn hợp đều đơn chức, no, mạch hở dạng CnH2nO2.
Sơ đồ tỉ lệ phản ứng tạo este (este hóa); 2.axit + 1C3H6(OH)2 → 1este + 2H2O.
→ Quy đổi X về hỗn hợp gồm axit + ancol – H2O → có ngay số mol axit lúc này là 0,1 mol.
Góc nhìn:
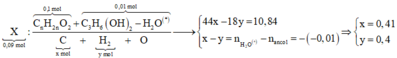
Đốt 0,09 mol X cần 0,48 mol O2 thu 0,41 mol CO2 + 0,4 mol H2O
→ Bảo toàn khối lượng có m X = 9 , 88 gam; bảo toàn nguyên tố O ta có: n O t r o n g X = 0 , 26 mol.
Biết số mol O trong X, quay lại góc nhìn → giải ra: n a n c o l = 0 , 07 mol và n H 2 O ( * ) = 0 , 08 mol
⇒ m a x i t = 9 , 88 + 0 , 08 . 18 - 0 , 7 . 76 = 6 gam, lại có số mol axit là 0,1 mol
Theo đó, trong phản ứng –COOH + KOH → ‒COOK + H2O, ta dùng tăng giảm khối lượng:
m= 6+0,1.(39-1)= 9,8 gam.

Chọn B.
Khi cho 0,06 mol M tác dụng với NaOH thì: 
Hỗn hợp ancol G gồm Y (0,04 mol) và Z (0,06 mol) Þ số nguyên tử C trong G là 3.
Vì MY > MZ nên Y là CH2=CH-CH2OH và Z là CH≡C-CH2OH.
Xét a gam M có 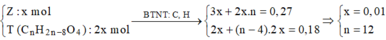
Vậy T là C12H16O4 (0,02 mol) có %mT = 88,89%.

Chọn A.
Khi đốt cháy A ta có:
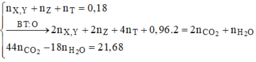
& 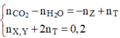 Þ CO2: 0,82 ; H2O: 0,8 và nX, Y = 0,04 ; nZ = 0,06 ; nT = 0,08
Þ CO2: 0,82 ; H2O: 0,8 và nX, Y = 0,04 ; nZ = 0,06 ; nT = 0,08
→
B
T
K
L
m
A
=
19
,
76
(
g
)
. Khi đó: mmuối = ![]() = 21,56 (g)
= 21,56 (g)
(với ![]() )
)
Vậy trong 14,82 gam A có m = 16,17 (g)

Chọn A
T là este của X, Y với Z nên X cũng đơn chức.
Muối E gồm XCOONa và YCOONa
→ n(XCOONa) = n(CO2) – n(H2O) = 0,06
Trong 6,9 gam M đặt:
X là CnH2n-2O2 ( u mol)
T là CmH2m-4O4 (v mol)
→ u + v = 0,06 1
m(M) = u14n + 30) + v14m + 60) = 6,9 2
Trong phản ứng đốt cháy:
n(X) + 2n(T) = n(CO2) – n(H2O) = 0,03
→ n(O) = 2n(X) + 3n(T) = 0,06
Áp dụng ĐLBT nguyên tố O → n(O2) = 0,105
Áp dụng ĐLBT khối lượng → m(M) = 2,3 → Trong phản ứng xà phòng hóa đã dùng lượng M nhiều gấp 6,9/2,3 = 3 lần phản ứng cháy.
→ n(CO2) = (nu + mv)/3 = 0,1 3
Giải 12 và 3 → u = 0,03; v = 0,03
nu+ mv = 0,3
→ n +m = 10
Do n ≥ 3 và m ≥ 6 và m≥ n + 3 → n = 3; m = 7 là nghiệm duy nhất.
X là CH2=CH-COOH 0,03)
T là CH2=CH-COO-CH2-CH2-OOC-CH30,03)
→%T = 68,7%

Chọn D.
Khi đốt cháy T, có:
![]()
Nhận thấy: n - C O O N a = n C O 2 + n N a 2 C O 3 Þ muối thu được có số C = số nhóm chức
mà ![]() 2 muối đó là HCOONa (0,4) và (COONa)2 (0,15)
2 muối đó là HCOONa (0,4) và (COONa)2 (0,15)
Khi thuỷ phân A thì: ![]()
Ta có: 31,7 < Mancol < 63,4 Þ Hai ancol thu được gồm CH3OH (0,5) và C2H4(OH)2 (0,1)
Các este thu được gồm HCOOCH3 (0,2); (HCOO)2C2H4 (0,1); (COOCH3)2 (0,15)
Vậy %mZ = 42,65% (tính theo (COOCH3)2 là lớn nhất).

Chọn A.
Đặt
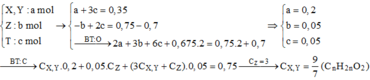
A. Sai, Khối lượng X, Y có trong 24 gam M là (14n + 32).0,2 = 10 (g) Þ 12 gam M có 5 gam X, Y.
B. Đúng, Số mol este T trong 24 gam M là 0,05 mol.
C. Đúng, BTKL: 24 + 0,35.56 = m + 92.0,1 + 0,2.18 Þ m = 30,8 gam.
D. Đúng, X là HCOOH có %mH = 4,35%