Dung dịch glucose (C6H12O6) 5%, có khối lượng riêng là 1,02 g/mL, phản ứng oxi hoá 1 mol
glucose tạo thành CO2 (g) và H2O (l) toả ra nhiệt lượng là 2 803,0 kJ. Một người bệnh được
truyền một chai chứa 500 mL dung dịch glucose 5%. Năng lượng tối đa từ phản ứng oxi hóa hoàn
toàn glucose mà bệnh nhân đó có thể nhận được là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Khối lượng dung dịch CuSO 4 : m dd CuSO 4 = 1,12 x 50 = 56 (gam).
CuSO 4 + Fe → FeSO 4 + Cu
64x — 56x = 5,16 - 5 = 0,16 (gam) => x = 0,02 mol.
m CuSO 4 tham gia phản ứng = 0,02 x 160 = 3,2 (gam);
100 gam dung dịch CuSO 4 có 15 gam CuSO 4 nguyên chất.
56 gam dung dịch CuSO 4 có X gam CuSO 4 nguyên chất.
x = 56 x 15/100 = 8,4g; m CuSO 4 còn lại = 8,4 - 3,2 = 5,2g
m FeSO 4 = 0,02 x 152 = 3,04g
m dd sau p / u = 56 - 0,16 = 55,84g
C % CuSO 4 = 5,2/55,84 x 100% = 9,31%
C % FeSO 4 = 3,04/55,84 x 100% = 5,44%

a, \(Fe+CuSO_4\rightarrow FeSO_4+Cu\)
____x_______x________x_____x (mol)
b, Ta có: m lá sắt tăng = mCu - mFe
⇒ 2,58 - 2,5 = 64x - 56x
⇒ x = 0,01 (mol)
Ta có: mCuSO4 = 25.1,12 = 28 (g) \(\Rightarrow n_{CuSO_4}=\dfrac{28.15\%}{160}=0,02625\left(mol\right)\)
Theo PT: \(n_{FeSO_4}=n_{CuSO_4\left(pư\right)}=n_{Cu}=0,01\left(mol\right)\)
Có: m dd sau pư = 2,5 + 28 - 2,58 = 27,92 (g)
Dung dịch sau pư gồm: FeSO4: 0,01 (mol) và CuSO4: 0,01625 (mol)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeSO_4}=\dfrac{0,01.152}{27,92}.100\%\approx5,44\%\\C\%_{CuSO_4}=\dfrac{0,01625.160}{27,92}.100\%\approx9,31\%\end{matrix}\right.\)


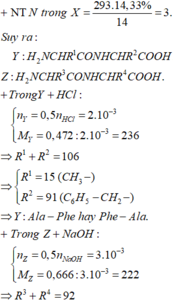







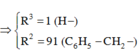



\(Q=500\cdot1,02\cdot0,05:180\cdot2803=397,091\left(kJ\right)\)