Cho 3,6 gam Mg vào 140ml dung dịch H2SO4 1,2 M tính nồng đồ mol của các chất trong dung dịch sau phản ứng
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nMg = 3,6/24 = 0,15 mol; nFeCl3 = 0,25.1 = 0,25 mol
Mg + 2FeCl3 → MgCl2 + 2FeCl2
0,125dư 0,025←0,25 → 0,125 → 0,25 (mol)
Mg + FeCl2 → MgCl2 + Fe
0,025→0,025 →0,025→0,025 (mol)
Vậy chất rắn sau phản ứng là Fe: nFe = 0,025 mol
=> m = mFe = 0,025.56 = 1,4 (gam)
Dung dịch X sau phản ứng gồm:
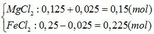
Nồng độ của các chất trong dung dịch X:
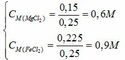

nH2SO4=0,168mol
nMg=0,15mol
PTHH: Mg+H2SO4=>MgSO4+H2
0,15: 0,168 => n H2SO4 dư theo n Mg
p/ư: 0,15->0,15------>0,15--->0,15
=> CmMgSO4=0,15:0,14=1,1M
nMg = 3.6 : 24 = 0.15 mol
nH2SO4 = 0.14 x 1.2 = 0.168 mol
Mg + H2SO4 -> MgSO4 + H2
Mg pư hết , H2SO4 pư dư => Tính theo số mol của Mg
Vdd = 3.6 + 140 - 0.15 x 2 = 143.3 ml = 0.1433l
CM MgSO4 = 0.15 : 0.1433 = 1.05M
CM H2SO4 = ( 0.168-0.15) : 0.1433 = 0.13 M

n Al 2 SO 4 3 = 0,05/3 x 1 ≈ 0,017 mol
C M Al 2 SO 4 3 = 0,017/0,1 = 0,17M

a) nMg= 3,6/24=0,15(mol)
nHCl= (300.7,3%)/36,5= 0,6(mol)
PTHH: Mg + 2 HCl -> MgCl2 + H2
Ta có: 0,15/1 < 0,6/2
=> HCl dư, Mg hết => Tính theo nMg.
nY=nH2=nMgCl2=nMg=0,15(mol)
=>V(Y,đktc)=V(H2,đktc)=0,15.22,4=3,36(l)
b) mMgCl2=0,15.95= 14,25(g)
nHCl(dư)= 0,6- 0,15.2=0,3(mol)
=>mHCl(dư)=0,3.36,5= 10,95(g)
mddsau= mMg + mddHCl - mH2= 3,6+ 300 - 0,15.2= 303,3(g)
=>C%ddHCl(dư)= (10,95/303,3).100= 3,610%
C%ddMgCl2= (14,25/303,3).100=4,698%

a) $n_{Fe_2O_3} = \dfrac{24}{160} = 0,15(mol)$
$n_{H_2SO_4} =0,2.2,5 = 0,5(mol)$
b)
$Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O$
Vì :
$n_{Fe_2O_3} : 1 < n_{H_2SO_4} : 3$ nên $H_2SO_4$ dư
$n_{H_2SO_4\ pư} = 3n_{Fe_2O_3} = 0,45(mol)$
$n_{H_2SO_4\ dư} = 0,5 - 0,45 = 0,05(mol)$
c)
$n_{Fe_2(SO_4)_3} = n_{Fe_2O_3} = 0,15(mol)$
$C_{M_{Fe_2(SO_4)_3}} = \dfrac{0,15}{0,2} = 0,75M$
$C_{M_{H_2SO_4}} = \dfrac{0,05}{0,2} = 0,25M$

\(n_{Zn}=\dfrac{6.5}{65}=0.1\left(mol\right)\)
\(n_{H_2SO_4}=0.3\cdot1=0.3\left(mol\right)\)
\(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
\(0.1........0.1...........0.1.......0.1\)
\(\Rightarrow H_2SO_4dư\)
\(n_{H_2SO_4\left(dư\right)}=0.3-0.1=0.2\left(mol\right)\)
\(n_{ZnSO_4}=n_{H_2}=0.1\left(mol\right)\)
\(C_{M_{ZnSO_4}}=\dfrac{0.1}{0.3}=0.33\left(M\right)\)
\(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0.2}{0.3}=0.66\left(M\right)\)
\(a) Zn + H_2SO_4 \to ZnSO_4 + H_2\\ b) n_{Zn} = \dfrac{6,5}{65} = 0,1 < n_{H_2SO_4} =0,3 \to H_2SO_4\ dư\\ n_{H_2SO_4\ pư} = n_{ZnSO_4} = n_{Zn} = 0,1(mol)\\ n_{H_2SO_4\ dư} = 0,3 - 0,1 = 0,2(mol)\\ c) C_{M_{ZnSO_4}} = \dfrac{0,1}{0,3} = 0,33M\\ C_{M_{H_2SO_4}} = \dfrac{0,2}{0,3} = 0,67M\)

\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(n_{H_2SO_4}=0,2.1,5=0,3\left(mol\right)\)
PTHH: Mg + H2SO4 --> MgSO4 + H2
Xét tỉ lệ: \(\dfrac{0,2}{1}< \dfrac{0,3}{1}\) => Mg hết, H2SO4 dư
PTHH: Mg + H2SO4 --> MgSO4 + H2
0,2-->0,2------>0,2----->0,2
=> VH2 = 0,2.22,4 = 4,48 (l)
\(\left\{{}\begin{matrix}C_{M\left(MgSO_4\right)}=\dfrac{0,2}{0,2}=1M\\C_{M\left(H_2SO_4.dư\right)}=\dfrac{0,3-0,2}{0,2}=0,5M\end{matrix}\right.\)

PT: \(Zn+H_2SO_4\rightarrow ZnSO_4+H_2\)
a, Ta có: \(n_{Zn}=\dfrac{6,5}{65}=0,1\left(mol\right)\)
\(n_{H_2SO_4}=0,2.1=0,2\left(mol\right)\)
Xét tỉ lệ: \(\dfrac{0,1}{1}< \dfrac{0,2}{1}\). ta được H2SO4 dư.
Theo PT: \(n_{H_2SO_4\left(pư\right)}=n_{ZnSO_4}=n_{Zn}=0,1\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=0,2-0,1=0,1\left(mol\right)\)
b, Ta có: \(m_{ZnSO_4}=0,1.161=16,1\left(g\right)\)
c, \(C_{M_{H_2SO_4\left(dư\right)}}=\dfrac{0,1}{0,2}=0,5M\)
\(C_{M_{ZnSO_4}}=\dfrac{0,1}{0,2}=0,5M\)
Bạn tham khảo nhé!

\(n_{KOH}=\dfrac{400.7\%}{56}=0,5\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{100.19,6\%}{98}=0,2\left(mol\right)\)
PTHH: 2KOH + H2SO4 --> K2SO4 + 2H2O
Xét tỉ lệ: \(\dfrac{0,5}{2}>\dfrac{0,2}{1}\) => KOH dư, H2SO4 hết
PTHH: 2KOH + H2SO4 --> K2SO4 + 2H2O
0,4<----0,2-------->0,2
=> \(\left\{{}\begin{matrix}m_{KOH\left(dư\right)}=\left(0,5-0,4\right).56=5,6\left(g\right)\\m_{K_2SO_4}=0,2.174=34,8\left(g\right)\end{matrix}\right.\)
mdd sau pư = 400 + 100 = 500 (g)
=> \(\left\{{}\begin{matrix}C\%_{KOH.dư}=\dfrac{5,6}{500}.100\%=1,12\%\\C\%_{K_2SO_4}=\dfrac{34,8}{500}.100\%=6,96\%\end{matrix}\right.\)
$140ml=0,14l$
$n_{H_2SO_4}=0,14.1,2=0,168(mol)$
$n_{Mg}=\dfrac{3,6}{24}=0,15(mol)$
$Mg+H_2SO_4\to MgSO_4+H_2$
$n_{Mg}<n_{H_2SO_4}\to H_2SO_4$ dư
Theo PT: $n_{MgSO_4}=n_{H_2SO_4(pứ)}=n_{Mg}=0,15(mol)$
$\to n_{H_2SO_4(dư)}=0,168-0,15=0,018(mol)$
$\to\begin{cases} C_{M\,MgSO_4}=\dfrac{0,15}{0,14}\approx 1,07M\\ C_{M\,H_2SO_4(dư)}=\dfrac{0,018}{0,14}\approx 0,13M \end{cases}$
Mời các cao nhân chỉ điểm