Trước khi nén hỗn hợp khí trong xilanh của một động cơ có áp suất 1atm, nhiệt độ 50°C, thể tích xilanh là 600cm³. Sau khi nén thể tích giảm xuống còn 100cm³, áp suất là 8atm. Tính nhiệt độ khí sau khi nén?
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

: Đáp án C
Gọi ![]() lần lượt là áp suất,
lần lượt là áp suất,
thể tích và nhiệt độ của khối khí trong xilanh ở trạng thái ban đầu
![]()
![]()
Gọi ![]()
lần lượt là áp suất, thể tích và nhiệt độ của khối khí trong xilanh khi động cơ hoạt động.
![]()
Từ phương trình trạng thái của khí lí tưởng, ta có:
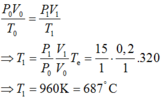

\(T_1=40^oC=313K\)
Thể tích ban đầu \(V_1\)
Thể tích lúc sau: \(V_2=\dfrac{1}{6}V_1\left(l\right)\)
Quá trình khí lí tưởng: \(\dfrac{p_1\cdot V_1}{T_1}=\dfrac{p_2\cdot V_2}{T_2}\)
\(\Rightarrow\dfrac{1\cdot V_1}{313}=\dfrac{10\cdot\dfrac{1}{6}V_1}{T_2}\)
\(\Rightarrow T_2=521,67K=248,67^oC\)

Áp dụng công thức p 1 V 1 T 1 = p 2 V 2 T 2
⇒ T 2 = p 2 . V 2 . T 1 p 1 . V 1 = 21.0 , 2. ( 273 + 47 ) 1 , 5.2 = 448 K
Mà T 2 = 273 + t 2 ⇒ t 2 = 175 0 C

Áp dụng công thức p 1 V 1 T 1 = p 2 V 2 T 2
⇒ T 2 = p 2 . V 2 . T 1 p 1 . V 1 = 21.0 , 2. ( 273 + 47 ) 1 , 5.2 = 448 K
Mà T 2 = 273 + t 2 ⇒ t 2 = 175 0 C

Áp dụng công thức p 1 V 1 T 1 = p 2 V 2 T 2
⇒ T 2 = p 2 . V 2 . T 1 p 1 . V 1 = 21.0 , 2. ( 273 + 47 ) 1 , 5.2 = 448 K
Mà T 2 = 273 + t 2 ⇒ t 2 = 175 0 C
600cm3 = 0,6l
100cm3 = 0,1l
Ta có
\(\dfrac{p_1V_1}{T_1}=\dfrac{p_2V_2}{T_2}\\ \Rightarrow T_2=\dfrac{p_2V_2.T_1}{p_1V_1}=\dfrac{8.0,1.323}{1.0,6}=430,6^oK\\ \Rightarrow t=157,6^o\)