hòa tan 9,875g một muối hidrocacbonat vào nước và cho tác dụng với một lượng H2SO4 vừa đủ thì thu được 8,25g một muối sunfat trung hòa khan. Tim công thức của muối
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


![]()
Sau phản ứng muối MCO3 chuyển thành MSO4
Cứ 1 mol MCO3 chuyển thành MSO4 khối lượng muối tăng lên một lượng là: 96 - 60 = 36 gam
Vậy nếu gọi số mol của MCO3 là x thì:
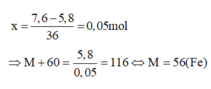
Đáp án D

Phải sửa lại đề thành 2,31 mới có thể giải ra đáp án
Gọi CTHH của A là R(HCO3)n
2R(HCO3)n + nH2SO4 → R2(SO4)n + 2nCO2 + 2nH2O
a 0,5a
mR(HCO3)n = a.(R + 61n) = 2,765 gam (1)
mR2(SO4)n = 0,5a.(2R + 96n) = 2,31 gam (2)
Chia hai vế của (1) và (2) cho nhau, có
(R + 61n)/[0,5(2R + 96n)] = 2,765/2,31
→ R = 18n
n = 1 → R = 18, vậy R là NH4, muối là NH4HCO3
15,8 gam NH4HCO3 → nNH4HCO3 = 0,2 mol
NH4HCO3 + HNO3 → NH4NO3 + CO2 + H2O
→ nNH4NO3 = 0,2 mol → mNH4NO3 = 16 gam < 37,6 gam muối B
→ B là muối ngậm nước, có dạng là NH4NO3.nH2O
nB = nNH4NO3 = 0,2 mol
→ MB = 37,6/0,2 = 188 g/mol → 80 + 18.n = 188 → n = 6
Vậy muối B là NH4NO3.6H2O

10 ml dung dịch RSO4 cần 0,003 mol BaCl2
![]() 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
50 ml dung dịch RSO4 cần 0,015 mol BaCl2
![]() RSO4 = 1,8/0,015
RSO4 = 1,8/0,015 ![]() R = 24
R = 24
![]() R là Mg
R là Mg
![]() Chọn C
Chọn C

Đáp án C
10 ml dung dịch RSO4 cần 0,003 mol BaCl2
=> 50 ml dung dịch RSO4 cần 0,015 mol BaCl2
=> RSO4 = 1,8/0,015 => R = 24 R là Mg

\(2NaBr+Cl_2\rightarrow2NaCl+Br_2\left(1\right)\\ m_{giảm}=m_{Br_2}-m_{Cl_2}\\ \Leftrightarrow n_{NaCl\left(1\right)}=n_{NaBr\left(1\right)}=\dfrac{13,35}{160-71}=0,15\left(mol\right)\\ \Rightarrow\%m_{NaBr}=\dfrac{103.0,15}{42,6}.100\approx36,268\%\\ \Rightarrow\%m_{NaCl}\approx63,732\%\)
Bổ sung:
\(C\%_{ddNaBr\left(trongA\right)}=\dfrac{0,15.103}{200}.100=7,725\%\\ C\%_{ddNaCl\left(trongA\right)}=\dfrac{42,6-0,15.103}{200}.100=13,575\%\)

- Giả sử khối lượng dung dịch axit là 100 g .
=> nH2SO4 = 0,05 ( mol )
\(R_2O_n+nH_2SO_4\rightarrow R_2\left(SO_4\right)_n+nH_2O\)
.0,05/n......0,05.............0,05/n.......0,05.............
=> mddsau = \(100+\dfrac{0,05}{n}\left(2R+16n\right)=100,8+\dfrac{R}{10n}\left(g\right)\)
=> \(5,882\%=\dfrac{\dfrac{0,05}{n}\left(2R+96n\right)}{100,8+\dfrac{R}{10n}}.100\%\)
=> \(R=11,99617501n\)
Lập bảng giá trị ta được : ( R; n ) = ( ~24; 2 ) TM .
Vậy công thức oxit là MgO .
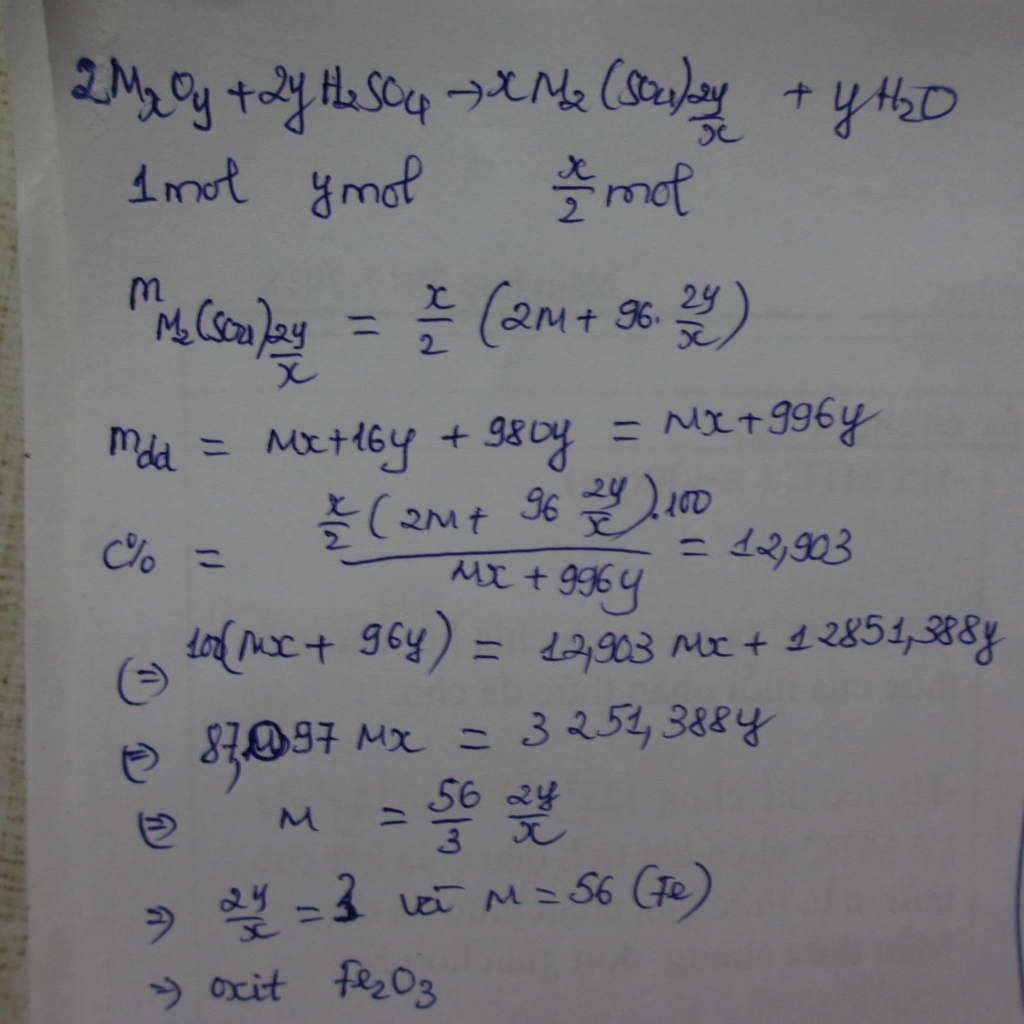
2R-HCO3 + H2SO4 -----> (R)2SO4 + 2CO2 + 2H2O
Từ 1 mol R -HCO3 ------> 1/2 mol (R)2SO4 thì khối lượng giảm: 61 - 96/2 = 13 gam
Vậy n R- HCO3 = ( 9,875 - 8,25 )/ 13 = 0,125 mol
M R-HCO3 = 79 => R = 18 => NH4+
X: NH4HCO3