một hợp chất A gồm 2 nguyên tố hóa học là lưu huỳnh và Oxi trong đó lưu huỳnh chiếm 40% theo khối lượng. Hãy tìm CTHH của khí A, biết rằng ở đktc 1 gam khí A chiểm thế tích là 0,28l
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


a) Phương trình hóa học S + O2 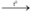 SO2
SO2
b) nS = 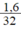 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 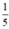 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l

a) Phương trình hóa học của S cháy trong không khí:
S + O2 → SO2
b. Số mol của S tham gia phản ứng:
nS = = 0,05 mol
Theo phương trình hóa học, ta có: = nS =
= 0,05 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Tương tự thể tích khí oxi cần dùng ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần là:
=> Vkk = 5 = 5 . 1,12 = 5,6 lít

a) MA = 32.2 = 64(g/mol)
\(m_S=\dfrac{64.50}{100}=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=64-32=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTHH: SO2
b) MA = 2.17 = 34 (g/mol)
\(m_H=\dfrac{34.5,88}{100}=2\left(g\right)=>n_H=\dfrac{2}{1}=2\left(mol\right)\)
\(m_S=34-2=32\left(g\right)=>n_S=\dfrac{32}{32}=1\left(mol\right)\)
=> CTHH: H2S

Bài 2: gọi CTHH của A là SxOy
tỉ khối so với kk =2,759
=> PTK của A là 2,759.29=80g/mol
ta có M (S) trong A là 80:100.40=32g/mol
=> số phân tử S là x= 32:32=1
=> M(O) trong A là 80-32=49g/mol
=> số phan tử O là y=48:16=3
=> công thức HH: SO3
1) Gọi CTHH của hợp chất đó là CxOy
Ta có
mC/mO=3/5
->12.x/16.y=3/5
->x/y=3/5:12/16=4/5
->x=4,y=5
->CTHH:C4O5
2)Gọi CTHH là SxOy
dA/kk=MA/29=2,759
->MA=2,759.29=80
%A=%S+%O
=40%+%O=100%
->%O=100%-40%=60%
x:y=40/32:60/16=1:3
->x=1,y=3
->(32+16.3)n=80
->80n=80->n=1
->CTHH:SO3

Bài 5) Gọi công thức hoá học của hợp chất là: AlxOy...
Theo đề bài ra ta có:
MAl : MO = 27x : 16y = 4,5 : 4
<=> 72y = 108x => x : y = 2 : 3 ( Chọn x = 2 , y = 3 )
Vậy công thức hoá học của hợp chất là : Al2O3
1) Gọi công thức hóa học của hợp chất là: FexSyOz
Theo đề bài ra ta có:
Khối lượng của Fe trong hợp chất là: 56 . 2 = 112 (g)
Khối lượng của hợp chất là: \(\frac{112.100\%}{28\%}\) = 400 (g)
Khối lượng của nguyên tử S trong hợp chất là: \(\frac{400.24\%}{100\%}\) = 96 (g)
Số nguyên tử S trong hợp chất là: 96 : 32 = 3 (nguyên tử)
Khối lượng của nguyên tử O trong hợp chất là: 400 - 112 - 96 = 192 (g)
Số nguyên tử O trong hợp chất là: 192 : 16 = 12 (nguyên tử)
\(\Rightarrow\) Công thức hóa học của hợp chất là: Fe2(SO4)3

mS = 80 . 40% = 32 (g)
nS = 32/32 = 1 (mol)
mO = 80 - 32 = 48 (g)
nO = 48/16 = 3 (mol)
CTHH: SO3

e lạy mấy a, mấy chị vào giải dùm e bài này với ạ!!
trời đậu!!

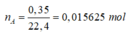
M A = m A n A = 1 0,015625 = 64 g / m o l
- Tìm số mol nguyên tử S, O trong phân tử A
Cứ 1 mol phân tử A có:
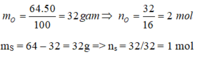
Suy ra trong 1 phân tử A có 1S và 2O, công thức của A là SO 2
Đáp án: C


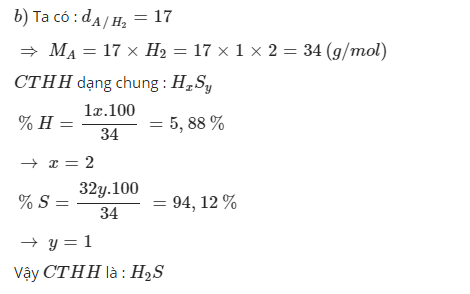
\(M_A=\dfrac{1}{\dfrac{0,28}{22,4}}=80\left(g/mol\right)\)
\(m_S=\dfrac{40.80}{100}=32\left(g\right)\Rightarrow n_S=\dfrac{32}{32}=1\left(mol\right)\)
\(m_O=80-32=48\left(g\right)\Rightarrow n_O=\dfrac{48}{16}=3\left(mol\right)\)
=> CTHH: SO3