Cho 2,24lit halogen X2 ở đktc tác dụng vừa đủ với magie thu được 9,5 g mgX2 .tìm nguyên tố halogen X
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


\(X_2+Mg\rightarrow MgX_2\)
0,1__________0,1
\(n_{X2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(M_{MgX2}=\frac{9,5}{0,1}=95\)
\(\Rightarrow X=35,5\left(Cl\right)\)

Đáp án B
Mg + X2 → MgX2
2Al + 3X2→ 2AlX3
Bảo toàn nguyên tố X:
2nMgX2 = 3nAlX3 => 2.9,5/(24 + 2X) = 3.8,9/(27 + 31X) => X = 35,5 (Cl)

Chọn đáp án B
Bảo toàn nguyên tố X:
2 n M g X 2 = 3 n A l X 3
=> 2 9 , 24 + 2 X = 3 8 , 9 27 + 31 X
=> X = 35,5 (Cl)

\(m_{HX}=\dfrac{10,95.200}{100}=21,9\left(g\right)\)
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 6HX --> 2AlX3 + 3H2
0,2--->0,6-------------->0,3
=> \(M_{HX}=\dfrac{21,9}{0,6}=36,5\left(g/mol\right)\)
=> X là Cl
VH2 = 0,3.22,4 = 6,72(l)

\(X2+nCu-->Cu_nX2\)( n là hóa trị của X nha)
\(n_{X2}=\frac{2,24}{22,4}=0,1\left(mol\right)\)
\(n_{Cu_nX2}=n_{X2}\Rightarrow\frac{22,4}{64n+2X}=0,1\)
\(\Rightarrow22,4=6,4n+0,2X\)
\(\Rightarrow0,2X=22,4-6,4x\)
\(X=\frac{22,4-6,4n}{0,2}\)
\(+n=1\Rightarrow X=80\left(Br\right)\)
Vậy X là Br

Bảo toàn khối lượng ta có: $m_{R}=2,4(g)$$R+X_2\rightarrow RX_2$
Ta có: $\frac{2,4}{R}=\frac{4,26}{2X}$
Lập bảng biện luận thông qua halogen tìm được X và R lần lượt là Cl và Ca
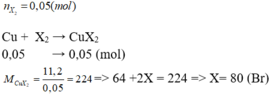
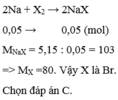
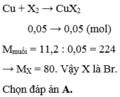
Mg + X2 -> MgX2
nX2 = 2,24/22,4 = 0,1 ( mol )
=> nMgX2 = 0,1 ( mol )
=> M = 9,5 / 0,1 = 95 ( đvC )
mà : MgX2 = 24 + X.2 = 95
=> X = 35,5 ( Cl )
Đó là Clo
nX2 = 2,24/22,4 = 0,1 (mol)
PTHH: Mg + X2 -> (t°) MgX2
nMgX2 = nX2 = 0,1 (mol)
M(MgX2) = 9,5/0,1 = 95 (g/mol)
<=> 24 + X . 2 = 95
<=> X = 35,5
<=> X là Cl