Cho a gam hỗn hợp Mg,Al,Zn chia thành 2 phần bằng nhau
-Phần 1: tác dụng với H2SO4 loãng dư thu được 5,6 lít khí H2
-Phần 2: tác dụng với O2 dư thu được 11,15g oxit kim loại Tính a
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Các PTHH :
2Al + 3 H 2 SO 4 → Al 2 SO 4 3 + 3 H 2 (1)
2Al + 6 H 2 SO 4 → Al 2 SO 4 3 + 3 SO 2 + 6 H 2 O (2)
Cu + 2 H 2 SO 4 → Cu SO 4 + 2 H 2 O + SO 2 (3)
Theo PTHH (1) số mol Al tham gia phản ứng bằng 2/3 số mol H 2 => Khối lượng AI trong hỗn hợp : 2×2/3×0,06×27 = 2,16(g)
Số mol SO 2 được giải phóng bởi Al: 2,16/27 x 3/2 = 0,12 mol
Theo PTHH (2) và (3) số mol SO 2 giải phóng bởi Cu : 2.0,1 - 0,12 = 0,08 (mol)
Theo PTHH (3) khối lượng Cu trong hỗn hợp : 0,08. 64 = 5,12 (g)
Vậy m = 2,16 + 5,12 = 7,28 (g).

Đáp án C
Phần 1: Tác dụng vói dung dịch H2SO4 loãng gồm Al và FexOy nên n H 2 = 3 2 n Al ⇒ n Al = 0 , 02
Phần 2: Thực hiện phản ứng nhiệt nhôm hoàn toàn và hỗn hợp B tác dụng với dung dịch NaOH dư có H2 nên B có Fe, A12O3 và Al dư. Có n Al du = 2 3 n H 2 ( NaOH ) = 0 , 004 .
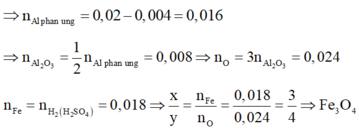

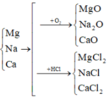
Gọi số mol Mg, R trong mỗi phần là a, b (mol)
=> 24a + b.MR = 16 (1)
* Nếu R tan trong HCl
- Phần 1:
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: Mg + 2HCl --> MgCl2 + H2
a-------------------->a
2R + 2nHCl --> 2RCln + nH2
b--------------------->0,5bn
=> a + 0,5bn = 0,4 (2)
-Phần 2: \(n_{SO_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
PTHH: Mg + 2H2SO4 --> MgSO4 + SO2 + 2H2O
a-------------------------->a
2R + 2mH2SO4 --> R2(SO4)m + mSO2 + 2mH2O
b----------------------------->0,5bm
=> a + 0,5bm = 0,5 (3)
(3) - (2) => 0,5bm - 0,5bn = 0,1 (mol)
=> bm - bn = 0,2 => m > n
- Xét n = 1; m = 2 => b = 0,2 (mol) => a = 0,3 (mol)
(1) => MR = 44 (g/mol) => Loại
- Xét n = 1; m = 3 => b = 0,1 (mol) => a = 0,35 (mol)
(1) => MR = 76 (g/mol) => Loại
- Xét n = 2; m = 3 => b = 0,2 (mol) => a = 0,2 (mol)
(1) => MR = 56 (g/mol) => R là Fe
* Nếu R không tan trong HCl
- Phần 1:
PTHH: Mg + 2HCl --> MgCl2 + H2
0,4<--------------------0,4
=> a = 0,4 (mol)
- Phần 2:
PTHH: Mg + 2H2SO4 --> MgSO4 + SO2 + 2H2O
0,4-------------------------->0,4
2R + 2kH2SO4 --> R2(SO4)k + kSO2 + 2kH2O
\(\dfrac{0,2}{k}\)<--------------------------0,1
Có: \(m_{R\left(phần.2\right)}=16-0,4.24=6,4\left(g\right)\)
=> \(M_R=\dfrac{6,4}{\dfrac{0,2}{k}}=32k\left(g/mol\right)\)
Xét k = 2 thỏa mãn => MR = 64 (g/mol) => R là Cu

Đáp án A
Có
Vì các kim loại trong hỗn hợp X có hóa trị không đổi và khối lượng mỗi phần đều là 11 gam nên số mol electron trao đổi ở mỗi phần là như nhau.
Áp dụng định luật bảo toàn khối lượng ta có:
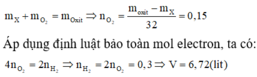

Đáp án : A
P1 : ne trao đổi = nNO2 = 0,47 mol
P2 : ne trao đổi = nCl2 .2 => nCl2 pứ = 0,235 mol
=> mKL = mmuối – mCl2 pứ = 11,19g
=> m = 2.11,19 = 22,38g

\(\text{Mỗi phần,gọi :} n_{Al} = a ; n_{Fe} = b ; n_{Cu} = c\\ \Rightarrow 27a + 56b + 64c = \dfrac{35,8}{2} = 17,9(1)\\ \text{Phần 1 : Al,Fe không phản ứng với axit đặc nguội}\\ Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + H_2O\\ n_{Cu} = c = n_{SO_2} = \dfrac{3,36}{22,4} = 0,15(2)\\ \text{Phần 2 : Cu không phản ứng với axit loãng}\\ 2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2\\ Fe + H_2SO_4 \to FeSO_4 + H_2\\ n_{H_2} = 1,5a + b = \dfrac{5,6}{22,4} = 0,25(3)\\ (1)(2)(3) \Rightarrow a = b = 0,1 ; c = 0,15\)
Suy ra :
\(m_{Al} = 0,1.2.27 = 5,4(gam)\\ m_{Fe} = 0,1.2.56 = 11,2(gam)\\ m_{Cu} = 0,15.64.2 = 19,2(gam)\)
\(n_{H_2}=n_O=0,25\left(mol\right)\\\dfrac{a}{2}=11,15-0,25.16\\ =>a=14,3\left(g\right)\)