Trộn 6,48 gam Al với 16 gam Fe2O3. Thực hiện phản ứng nhiệt nhôm được chất rắn A. Khi cho A tác dụng với dung dịch NaOH dư, có 2,688 lít H2 (đktc) thoát ra. Tính hiệu suất phản ứng nhiệt nhôm
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
8 Al + 3 Fe 3 O 4 → t o 4 Al 2 O 3 + 9 Fe
Khối lượng nhôm giảm chính là khối lượng nhôm đã tham gia phản ứng.
⇒ n Al phan ung = 0 , 81 27 = 0 , 03 ⇒ n Fe 3 O 4 = 3 8 n Al phan ung = 0 , 01125
Vì A tác dụng với dung dịch NaOH có H2 nên A có chứa Al dư và
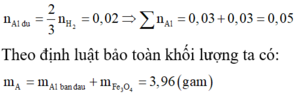

Đáp án A
n Al dư = 2nH2 / 3 = 0,1 mol
⇒ H = (0,25 – 0,1)/0,25 .100%= 60%
2Al + Fe2O3 → Al2O3 +2Fe
0,15
⇒ mZ = 160.(0,15 – 0,075) + 56.0,15 = 20,4 g
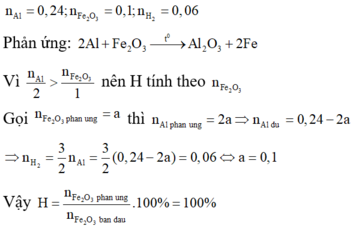
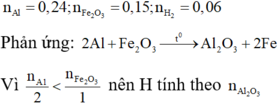
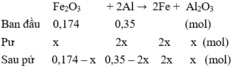



\(n_{Al}=\dfrac{6,48}{27}=0,24\left(mol\right)\)
\(n_{Fe_2O_3}=\dfrac{16}{160}=0,1\left(mol\right)\)
PTHH: \(2Al+Fe_2O_3\underrightarrow{t^o}Al_2O_3+2Fe\)
Xét tỉ lệ: \(\dfrac{0,24}{2}>\dfrac{0,1}{1}\) => Hiệu suất tính theo Fe2O3
Gọi số mol Fe2O3 phản ứng là a (mol)
\(n_{H_2}=\dfrac{2,688}{22,4}=0,12\left(mol\right)\)
PTHH: 2Al + Fe2O3 --to--> Al2O3 + 2Fe
2a<----a
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
0,08<------------------------------------0,12
=> 2a + 0,08 = 0,24
=> a = 0,08 (mol)
=> \(H\%=\dfrac{0,08}{0,1}.100\%=80\%\)