Hòa tan x gam hỗn hợp bột gồm 2 kim loại Mg và Al vào y gam dung dịch HNO3 24%. Sau phản ứng thu được dung dịch A (không chứa muối amoni) và 0,896 lít hỗn hợp X gồm 3 khí không màu có khối lượng 1,4 gam. Thêm một lượng O2 vừa đủ vào X, phản ứng xong thu được hỗn hợp khí Y. Dẫn Y từ từ qua dung dịch NaOH dư thấy còn lại khí Z (có tỉ khối hơi của Z so với H2 bằng 20). Nếu cho từ từ dung dịch NaOH vào dung dịch A đến khi thu được lượng kết tủa lớn nhất thấy cân nặng 6,42 gam (không có khí thoát ra). Biết rằng HNO3 đã lấy dư 15% so với lượng cần thiết, các thể tích đều đo ở điều kiện tiêu chuẩn và các phản ứng đều xảy ra hoàn toàn, giá trị của x và y lần lượt là
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Xử lý hỗn hợp khí X: 3 khí đó
chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2
và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa
N2 và N2O với
MT.bình = 36 = MT.bình cộng của 2 khí.
⇒ nN2 = nN2O
Đặt nNO = a và nN2 = nN2O = b
Ta có hệ:
a + 2b = 0,04
& 30a + 28b + 44b = 1,32
⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận
= 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là
x và y ta có hệ:
(24+17×2).x + (27+17×3)y = 6,42
& 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol
⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ
⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2
= 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15
= 0,345 mol
⇒ mDung dịch HNO3 = 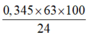
= 90,5625 gam

Đáp án A
Xử Lý hỗn hợp khí X: 3 khí đó chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2 và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa N2 và N2O với MTrung bình = 36 = MTrung bình cộng của 2 khí.
⇒ nN2 = nN2O || Đặt nNO = a và nN2 = nN2O = b ta có hệ:
a + 2b = 0,04 || 30a + 28b + 44b = 1,32 ||⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận = 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là x và y ta có hệ:
(24+17×2)x + (27+17×3)y = 6,42 || 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol ⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ ⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2 = 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15 = 0,345 mol.
⇒ mDung dịch HNO3 = 0 , 345 × 63 × 100 24 = 90,5625 gam

nZ = 0,2
Z gồm 2 khí không màu và có MZ = 7,4 ÷ 0,2 = 37
⇒ Trong Z có N2O (VìM = 44 > 37)
+TH1: Z gồm NO và N2O
Đặt nNO =a ; nN2O = b
nZ = a+b = 0,2 (1)
mZ = 30a + 44b = 7,4 (2)
Từ (1) và (2) ⇒ a = b = 0,1
Đặt nNH4+ = x ; nHNO3 ban đầu = y
Ta có nNO3- trong muối kl = ne = 8nN2O + 3n NO + 8nNH4NO3
Bảo toàn nguyên tố N: n HNO3 = n NO3- trong muối kl + n NO + 2nN2O + 2n NH4NO3
⇒ 10x + 4 . 0,1 + 10. 0,1 = y ⇒ 10x + 1,4 = y (*)
m muối = mNH4NO3 + mKL + mNO3-/muối kl
⇒ 80x + 25,3 + (8.0,1 + 3.0,1 + 8x ).62 = 122,3 (**)
Từ (*) và (**) ⇒ nHNO3 ban đầu = y = 1,9
Đáp án C
Tương tự với TH2: Z gồm N2 và N2O, không có đáp án thỏa mãn
Đáp án C.

Đáp án : B
Vì Z gồm 2 hợp chất không màu nên Z có NO và N2O
nZ = nNO + nN2O = 0,2 mol
Và mZ = 30nNO + 44nN2O = 7,4g
=> nNO = nN2O = 0,1 mol
Giả sử có tạo thành NH4NO3 x mol
=> bảo toàn e : ne trao đổi = nNO3 muối = 3nNO + 8nN2O + 8nNH4NO3 = 1,1 + 8x mol
=> mmuối = mKL + mNO3 muối + mNH4NO3
=> 122,3 = 25,3 + 62.( 1,1 + 8x) + 80x
=> x = 0,05 mol
=> nHNO3 = 4nNO + 10nN2O + 10nNH4NO3 = 1,9 mol

Đáp án C
Do thu được khí không màu và MZ = 37 ⇒ có 2 trường hợp.
TH1: Z gồm N2 và N2O. Đặt nN2 = x; nN2O = y
⇒ nZ = x + y = 0,2 mol; mZ = 28x + 44y = 7,4(g).
||⇒ giải hệ có: x = 0,0875 mol; y = 0,1125 mol. Đặt nNH4NO3 = a.
∑nNO3–/KL = ne = 10nN2 + 8nN2O + 8nNH4NO3 = (8a + 1,775) mol.
► mmuối khan = 25,3 + 62.(8a + 1,775) + 80a = 122,3(g) ⇒ a = – 0,02.. ⇒ loại!.
TH2: Z gồm NO và N2O. Đặt nNO = x; nN2O = y
⇒ nZ = x + y = 0,2 mol; mZ = 30x + 44y = 7,4(g).
||⇒ giải hệ có: x = y = 0,1 mol. Đặt nNH4NO3 = a.
∑nNO3–/KL = ne = 3nNO + 8nN2O + 8nNH4NO3 = (8a + 1,1) mol.
► mmuối khan = 25,3 + 62.(8a + 1,1) + 80a = 122,3(g) ⇒ a = 0,05 mol.
||⇒ nHNO3 = 4nNO + 10nN2O + 10nNH4NO3 = 1,9 mol


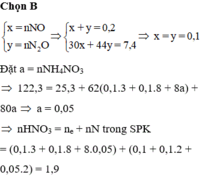

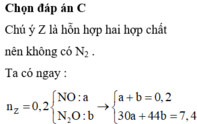
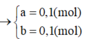
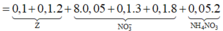
bn tham khảo nhé
kbt mình có sai gì k mà đoạn cuối lẻ vậy
