Câu 11. Phương pháp nào sau đây được dùng để sản xuất khí sunfurơ trong công nghiệp.
a. Phân hủy canxisunfat ở nhiệt độ cao .
b. Đốt cháy lưu huỳnh trong oxi .
c. Cho đồng tác dụng với axit sunfuric đặc, nóng.
d. Cho muối natrisunfit tác dụng với axit clohiđric.
Câu 12. Chất nào sau đây khi tan trong nước cho dung dịch, làm quỳ tím hóa đỏ :
a. KOH b. KNO3 c. SO3 d. CaO
Câu 13. Chất nào sau đây tác dụng với axit sunfuric loãng tạo thành muối và nước:
a. Cu b. CuO c. CuSO4 d. CO2
Câu 14. Canxioxit có thể làm khô khí nào có lẫn hơi nước sau đây:
a. Khí CO2 b. Khí SO2 c. Khí HCl d. CO
Câu 15. Một hỗn hợp rắn gồm Fe2O3 và CaO, để hòa tan hoàn toàn hỗn hợp này người ta phải dùng dư:
a. Nước. b. Dung dịch NaOH.
c. Dung dịch HCl. D. dung dịch NaCl.
Câu 16. Dung dịch axit mạnh không có tính nào sau đây:.
a. Tác dụng với oxit axit tạo thành muối và nước .
b. Tác dụng với bazơ tạo thành muối và nước .
. c. Tác dụng với nhiều kim loại giải phóng khí hiđrô.
d. Làm đổi màu quỳ tím thành đỏ.
Câu 17. Đơn chất nào sau đây tác dụng với H2SO4 loãng sinh ra chất khí :
a. Bạc b. Đồng c. Sắt d. cacbon.
Câu 18. Trong phòng thí nghiệm khí SO2 không thu bằng cách đẩy nước vì SO2 :
a. Nhẹ hơn nước b. Tan được trong nước.
c. Dễ hóa lỏng D. Tất cả các ý trên .
Câu 19. Để trung hòa 11,2gam KOH 20%, thì cần lấy bao nhiêu gam dung dịch axit H2SO435%
a. 9gam b. 4,6gam c. 5,6gam d. 1,7gam
Câu 20. Hòa tan 23,5 gam K2O vào nước. Sau đó dùng 250ml dung dịch HCl để trung hòa dung dịch trên. Tính nồng độ mol HCl cần dùng.
a. 1,5M b. 2,0 M c. 2,5 M d. 3,0 M.


 SO
SO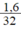 = 0,05 mol.
= 0,05 mol.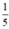 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là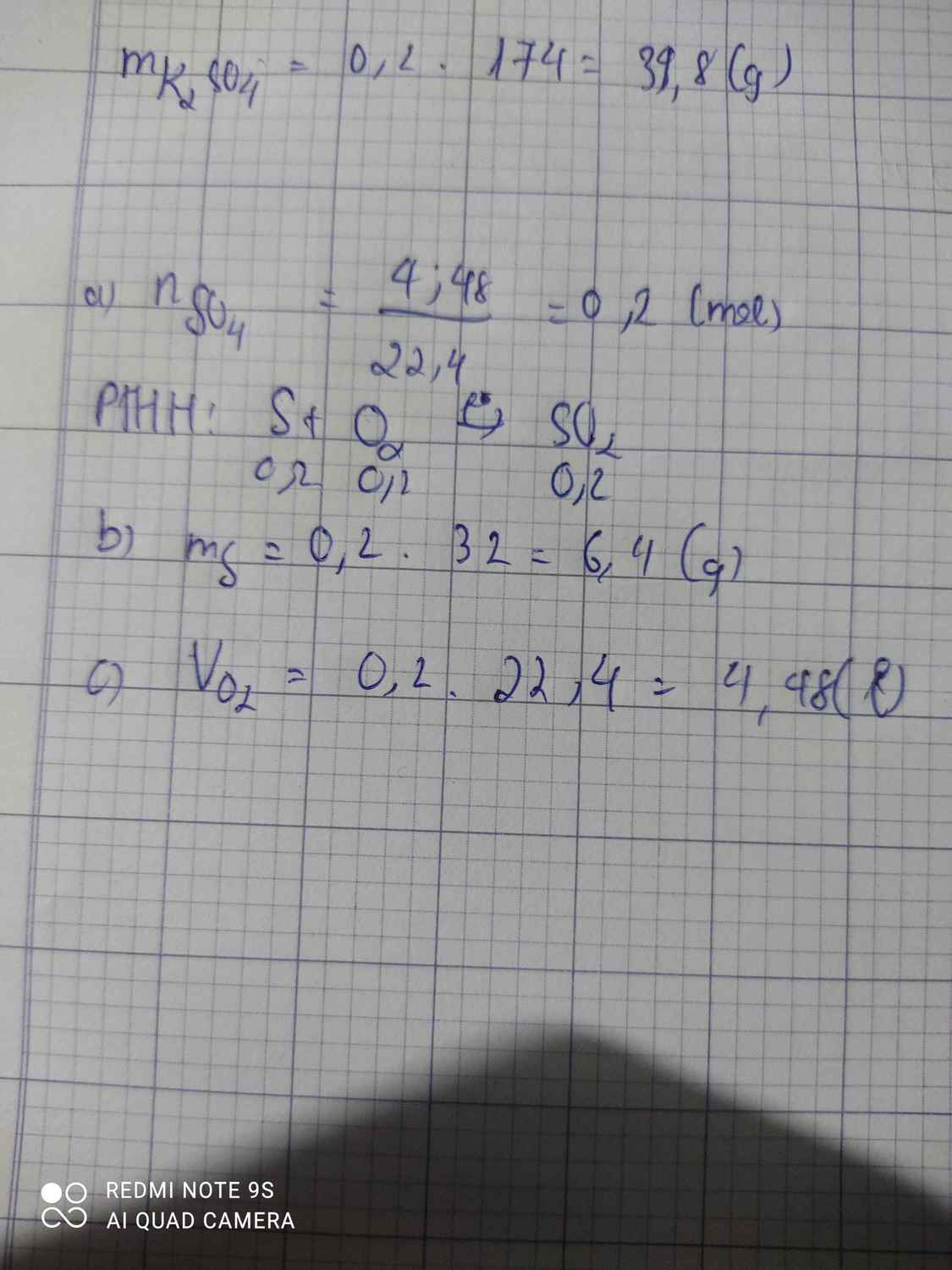
Câu 11. Phương pháp nào sau đây được dùng để sản xuất khí sunfurơ trong công nghiệp.
a. Phân hủy canxisunfat ở nhiệt độ cao .
b. Đốt cháy lưu huỳnh trong oxi .
c. Cho đồng tác dụng với axit sunfuric đặc, nóng.
d. Cho muối natrisunfit tác dụng với axit clohiđric.
Câu 12. Chất nào sau đây khi tan trong nước cho dung dịch, làm quỳ tím hóa đỏ :
a. KOH b. KNO3 c. SO3 d. CaO
Câu 13. Chất nào sau đây tác dụng với axit sunfuric loãng tạo thành muối và nước:
a. Cu b. CuO c. CuSO4 d. CO2
Câu 14. Canxioxit có thể làm khô khí nào có lẫn hơi nước sau đây:
a. Khí CO2 b. Khí SO2 c. Khí HCl d. CO
Câu 15. Một hỗn hợp rắn gồm Fe2O3 và CaO, để hòa tan hoàn toàn hỗn hợp này người ta phải dùng dư:
a. Nước. b. Dung dịch NaOH.
c. Dung dịch HCl. D. dung dịch NaCl.
Câu 16. Dung dịch axit mạnh không có tính nào sau đây:.
a. Tác dụng với oxit axit tạo thành muối và nước .
b. Tác dụng với bazơ tạo thành muối và nước .
. c. Tác dụng với nhiều kim loại giải phóng khí hiđrô.
d. Làm đổi màu quỳ tím thành đỏ.
Câu 17. Đơn chất nào sau đây tác dụng với H2SO4 loãng sinh ra chất khí :
a. Bạc b. Đồng c. Sắt d. cacbon.
Câu 18. Trong phòng thí nghiệm khí SO2 không thu bằng cách đẩy nước vì SO2 :
a. Nhẹ hơn nước b. Tan được trong nước.
c. Dễ hóa lỏng D. Tất cả các ý trên .
Câu 19. Để trung hòa 11,2gam KOH 20%, thì cần lấy bao nhiêu gam dung dịch axit H2SO4 35%
a. 9gam b. 4,6gam c. 5,6gam d. 1,7gam
---
Không có đáp án đúng
_____________
Câu 20. Hòa tan 23,5 gam K2Ovào nước. Sau đó dùng 250ml dung dịch HCl để trung hòa dung dịch trên. Tính nồng độ mol HCl cần dùng.
a. 1,5M b. 2,0 M c. 2,5 M d. 3,0 M.
Tham khảo