lưu huỳnh cháy ngoài không khí như thế nào ?
lưu huỳnh cháy trong oxi như thế nào?
giải thích tại sao lại có sự khác biệt đó hóa 8 bài thực hành 4
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Phương trình phản ứng hóa học :
S + O2 →→ SO2
b) Số mol lưu huỳnh tham gia phản ứng :
nS=3,232=0,1(mol)nS=3,232=0,1(mol)
Theo phương trình, ta có : nSO2 = nS = nO2 = 0,1 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Tương tự thể tích khí oxi cần dùng ở đktc là :
VO2 = 22,4.0,1 = 2,24 (l)
Vì khí oxi chiếm 20% về thể tích của không khí nên thể tích không khí cần dùng là :
Vkk = 5.VO2 = 5.2,24 = 11,2 (l)

a) Phương trình hóa học S + O2 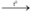 SO2
SO2
b) nS = 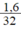 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 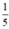 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l

Trong số những quá trình dưới đây, cho biết quá trình nào xảy ra hiện tượng hóa học? quá trình nào xảy ra hiện tượng vật lí? Giải thích.
(a) Lưu huỳnh cháy trong khí oxi tạo ra chất khí mùi hắc (lưu huỳnh đioxit).
=> Hiện tượng hóa học do có sự biến đổi về chất.
(b) Thủy tinh nóng chảy được thổi thành bình cầu.
=> Hiện tượng vật lí do không có sự biến đổi về chất mà chỉ biến đổi trạng thái.
(c) Trong lò nung đá vôi, canxi cacbonat chuyển dần thành vôi sống (canxi oxit) và khí cacbon đioxit thoát ra ngoài.
=> Hiện tượng hóa học do có sự biến đổi về chất.
(d) Cồn để trong lọ không kín bị bay hơi.
=> Hiện tượng vật lí do không có sự biến đổi về chất mà chỉ biến đổi trạng thái.
(e) Dây sắt được cắt thành từng đoạn nhỏ và tán đinh.
=> Hiện tượng vật lí do không có sự biến đổi về chất mà chỉ biến đổi trạng thái.
(f) Xích xe đạp bằng thép lâu ngày bị phủ một lớp gỉ màu đỏ nâu.
=> Hiện tượng hóa học do có sự biến đổi về chất.
(g) Để rượu nhạt lâu ngày ngoài không khí, rượu nhạt bị lên men thành giấm (axit axetic) chua.
=> Hiện tượng hóa học do có sự biến đổi về chất.
(h) Vào mùa đông, ở một số nơi trên trái đất có hiện tượng tuyết rơi.
=> Hiện tượng vật lí do không có sự biến đổi về chất mà chỉ biến đổi trạng thái.

A
Đưa lưu huỳnh đang cháy ngoài không khí vào bình đựng khí O 2 thì lưu huỳnh cháy sáng hơn, cho sản phẩm là S O 2 (lưu huỳnh đioxit).
![]()

Nguyên tử oxi có cấu hình e là 1s22s22p4, trong nguyên tử có 2 electron độc thân, do đó nó có thể ghép đôi với 2 electron độc thân khác, để đạt được cấu hình bền của khí hiếm, nên số oxi hoá của nó trong các hợp chất thường là -2. Để có được các số oxi hoá cao hơn, electron của oxi phải chuyển từ mức năng lượng 2p lên mức 3s, đây là điều khó khăn vì khoảng cách giữa hai mức năng lượng là xa nhau. Hợp chất tạo thành có năng lượng không đủ bù lại năng lượng đã mất đi do quá trình chuyển mức.
Ngược lại, lưu huỳnh có thể xuất hiện mức oxi hoá +4, +6 vì nguyên tử của chúng tương đối dễ dàng chuyển thành trạng thái kích thích. Năng lượng cần tiêu thụ cho quá trình kích thích được bù lại bởi năng lượng thoát ra khi tạo thành liên kết hoá học, nên các hợp chất lưu huỳnh +4 và +6 thường khá bền.

a) Phương trình hóa học của S cháy trong không khí:
S + O2 → SO2
b. Số mol của S tham gia phản ứng:
nS = = 0,05 mol
Theo phương trình hóa học, ta có: = nS =
= 0,05 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Tương tự thể tích khí oxi cần dùng ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần là:
=> Vkk = 5 = 5 . 1,12 = 5,6 lít

Bài 3 :
- PTHH : \(S+O_2\left(t^o\right)->SO_2\) (1)
- PƯ trên thuộc loại PƯ cháy vì ta phải đốt lưu huỳnh nên có sự cháy giữa lưu huỳnh và oxi
- Ta có : \(n_S=\dfrac{6,4}{32}=0,2\left(mol\right)\)
Từ (1) -> \(n_{O_2}=n_S=0,2\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=n.22,4=0,2.22,4=4,48\left(l\right)\)
Bài 4 :
- PTHH : \(3Fe+2O_2\left(t^o\right)->Fe_3O_4\) (2)
\(n_{Fe}=\dfrac{m}{M}=\dfrac{42}{56}=0,75\left(mol\right)\)
Từ (2) -> \(n_{O_2}=\dfrac{2}{3}n_{Fe}=0,5\left(mol\right)\)
=> \(V_{O_2\left(đktc\right)}=n.22,4=0,5.22,4=11,2\left(l\right)\)
Từ (2) -> \(n_{Fe_2O_3}=\dfrac{1}{3}n_{Fe}=0,25\left(mol\right)\)
=> \(m_{Fe_2O_3}=n.M=0,25.\left(56.2+16.3\right)=40\left(g\right)\)
S + O2------to---> SO2
Hiện tượng:Lưu huỳnh cháy trong không khí với ngọn lửa nhỏ, màu xanh nhạt; cháy trong khí oxi mãnh liệt hơn, tạo thành khí lưu huỳnh đioxit SO2 (còn gọi là khí sunfurơ)