Hỗn hợp X gồm Zn , Mg và Fe. Hòa tan hết 23,40 gam hỗn hợp X vào dung dịch HCl thu được 11,20 lit khí (dktc). Để tác dụng với vừa hết 23,40 g hỗn hợp X cần 12,32 lit khí Clo (dktc). Khối lượng của Fe trong hỗn hợp là :
A. 8,4g
B. 11,2g
C. 2,8g
D. 5,6g

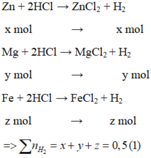
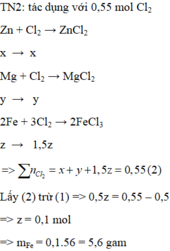
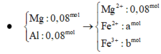
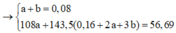
Đáp án : D
Bảo toàn e :
+) X + HCl : 2nZn + 2nMg + 2nFe = 2nH2 = 1,0 mol
+) X + Cl2 : 2nZn + 2nMg + 3nFe = 2nCl2 = 1,1 mol
=> nFe = 1,1 – 1,0 = 0,1 mol => mFe = 5,6g