Cho hỗn hợp gồm 0,02 mol Al và 0,01 mol Fe vào 800 ml dung dịch gồm AgNO3 0,08 M và Cu(NO3)2 0,5M. Sau khi kết thúc các phản ứng thu được m gam chất rắn. Giá trị của m là
A. 6,912
B. 7,224
C. 7,424
D. 7,092
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
nAg+ = 0,064 mol; nCu2+ = 0,4 mol; nNO3– = 0,864 mol.
Ta có: Al3+/Al > Fe2+/Fe > Cu2+/Cu > Fe3+/Fe2+ > Ag+/Ag.
⇒ các cation trong dung dịch xuất hiện theo thứ tự:
Al3+ → Fe2+ → Cu2+ → Fe3+ → Ag+.
► Ghép lần lượt các ion vào để thỏa bảo toàn điện tích:
Ghép 0,02 mol Al3+ và 0,01 mol Fe2+ vẫn chưa đủ.
⇒ ghép thêm (0,864 - 0,02 × 3 - 0,01 × 2) ÷ 2 = 0,392 mol Cu2+.
||⇒ Rắn gồm 0,064 mol Ag và (0,4 - 0,392 = 0,008) mol Cu
► m = 0,064 × 108 + 0,008 × 64 = 7,424(g)

Chọn đáp án C
Tổng số mol anion trong dung dịch được bảo toàn là ∑ n NO 3 - mol.
Lượng các nguyên tố kim loại và thứ tự trong dãy điện hóa:
0,02 mol Al > 0,01 mol Fe > 0,4 mol Cu > 0,064 mol Ag.
→ dung dịch sau phản ứng chứa: 0,02 mol Al(NO3)3 + 0,01 mol Fe(NO3)2 + 0,392 mol Cu(NO3)2.
→ m gam chất rắn thu được chứa 0,064 mol Ag và 0,008 mol Cu → m = 7,424 gam.

Đáp án C
![]()
![]()
Ta có
![]()
=> các cation trong dung dịch xuất hiện theo thứ tự:
![]()
Ghép lần lượt các ion vào để thoả bảo toàn điện tích:
Ghép 0,02 mol A l 3 + v à 0 , 01 m o l F e 2 + vẫn chưa đủ.
=> ghép thêm: (0,864 - 0,02.3 - 0,01.2) : 2 = 0,392 mol C u 2 +
=> Rắn gồm 0,064 mol Ag và (0,4 - 0,392 = 0,08) mol Cu
=> m = 0,064.108 + 0,008.64 = 7,424 (g)

Chọn C.
Hỗn hợp X gồm Al và Fe với số mol mỗi chất bằng 0,2 mol
Hỗn hợp Y gồm Cu(NO3)2 (0,2x mol) và AgNO3 (0,2y mol)
Hỗn hợp Z gồm Ag, Cu và Fe dư Þ nFe dư = 0,1 mol và 64.0,2x + 108.0,2y = 40,8 (1)
→ BT : e 0 , 2 . 3 + 2 . ( 0 , 2 - 0 , 1 ) = 0 , 2 x . 2 + 0 , 2 y (2). Từ (1), (2) suy ra: x = 1,5

Chọn C.
Hỗn hợp X gồm Al và Fe với số mol mỗi chất bằng 0,2 mol
Hỗn hợp Y gồm Cu(NO3)2 (0,2x mol) và AgNO3 (0,2y mol)
Hỗn hợp Z gồm Ag, Cu và Fe dư Þ nFe dư = 0,1 mol và 64.0,2x + 108.0,2y = 40,8 (1)
→ B T : e 0 , 2 . 3 + 2 . 0 , 2 - 0 , 1 = 0 , 2 x . 2 + 0 , 2 y 2
Từ (1), (2) suy ra: x = 1,5

Vì Z gồm 3 kim loại ⇒ Z gồm Ag, Cu, Fe.
+ Z phản ứng HCl dư ⇒ 0,05 mol H2 ⇒ nFedư = 0,05 mol
+ Sơ đồ bài toán ta có:

Đáp án A

Chọn đáp án A
Vì Z gồm 3 kim loại ⇒ Z gồm Ag, Cu, Fe.
+ Z phản ứng HCl dư ⇒ 0,05 mol H2 ⇒ nFedư = 0,05 mol
+ Sơ đồ bài toán ta có:
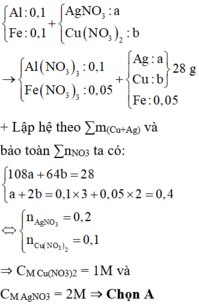

Chọn đáp án B
Do Al3+/Al > Fe2+/Fe > Cu2+/Cu > Fe3+/Fe2+ > Ag+/Ag ||⇒ Z gồm Fedư, Cu và Ag.
⇒ nFe dư = nH2 = 0,05 mol ||► Trong X có nAl = nFe = 8,3 ÷ (27 + 56) = 0,1 mol.
⇒ dung dịch sau phản ứng chứa 0,05 mol Fe(NO3)2 và 0,1 mol Al(NO3)3.
Đặt nCu(NO3)2 = x; nAgNO3 = y ⇒ ∑nNO3– = 2x + y = 0,05 × 2 + 0,1 × 3.
mrắn không tan = 64x + 108y = 28(g) ||⇒ Giải hệ có: x = 0,1 mol; y = 0,2 mol.
⇒ [Cu(NO3)2] = 1M; [AgNO3] = 2M ⇒ chọn B.
Đáp án C
nAg+ = 0,064 mol; nCu2+ = 0,4 mol;
nNO3– = 0,864 mol.
Ta có:
Al3+/Al > Fe2+/Fe > Cu2+/Cu > Fe3+/Fe2+ > Ag+/Ag.
⇒ các cation trong dung dịch xuất hiện theo thứ tự:
Al3+ → Fe2+ → Cu2+ → Fe3+ → Ag+.
► Ghép lần lượt các ion vào để thỏa bảo toàn điện tích:
Ghép 0,02 mol Al3+ và 0,01 mol Fe2+ vẫn chưa đủ.
⇒ ghép thêm (0,864 - 0,02 × 3 - 0,01 × 2) ÷ 2 = 0,392 mol Cu2+.
||⇒ Rắn gồm 0,064 mol Ag và (0,4 - 0,392 = 0,008) mol Cu
► m = 0,064 × 108 + 0,008 × 64 = 7,424(g)