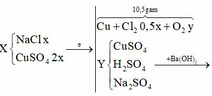
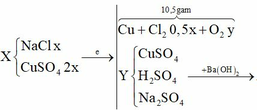
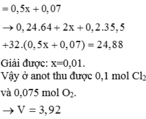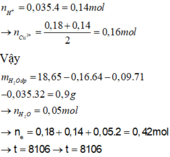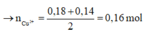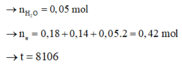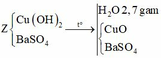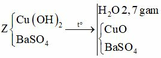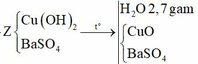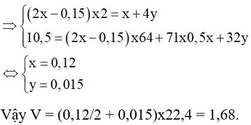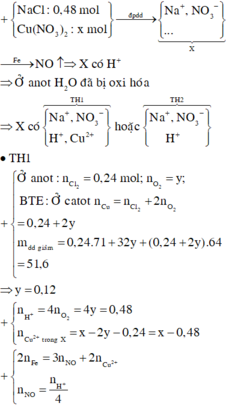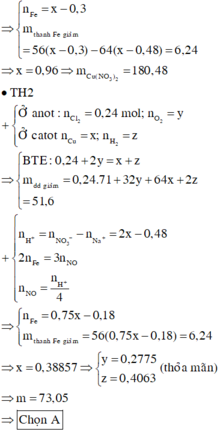Cho 60 gam tinh thể CuSO4.5H2O vào dung dịch NaCl, thu được dung dịch X. Tiến hành điện phân dung dịch X bằng điện cực trơ, màng ngăn xốp đến khi khối lượng dung dịch giảm 24,88 gam thì dừng điện phân, thu được dung dịch Y chỉ chứa hai chất tan và ở anot thoát ra V lít khí (đktc). Nhúng thanh Mg vào Y, kết thúc phản ứng, thấy khối lượng thanh Mg giảm 3,36 gam. Giá trị của V là
A. 4,032 lít
B. 3,584 lít
C. 3,920 lít
D. 3,808 lít