Nguyên tử của nguyên tố X có tổng số electron thuộc phân lớp p là 11. Điện tích hạt nhân của nguyên tử nguyên tố Y là +14,418.10-19C (cu-lông).
Liên kết giữa X và Y thuộc loại liên kết
A. cho - nhận.
B. ion.
C. kim loại.
D. cộng hóa trị có cực.
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
X có e cuối thuộc phân lớp s ⇒ nhóm A (I hoặc II).
Y có e cuối thuộc phân lớp p ⇒ nhóm A (III → VIII).
eX + eY = 20 ⇒ pX + pY = 20
Ta có: X chỉ có thể là: H (p = 1); He (p = 2); Na (p = 11) và K (p = 19).
⇒ Ta thấy chỉ có Na (p = 11) ⇒ pY = 9 (Flo) thỏa mãn.
⇒ X - Y: NaF (liên kết ion)

Đáp án : D
X có e cuối thuộc phân lớp s => nhóm A(I hoặc II)
Y có e cuối thuộc phân lớp p => nhóm A (III à VIII)
, eX + eY = 20 => pX + pY = 20
Ta có : X chỉ có thể là : H( p =1) ; He (p =2) ; Na(p = 11) và K(p = 19)
=> Ta thấy Chỉ có Na (p = 11) => pY = 9 (Flo) thỏa mãn
=> X – Y : NaF ( liên kết ion )

Chọn C
X là K (kim loại mạnh), Y là phi kim (phi kim mạnh)
Liên kết hóa học giữa X và Y là liên kết ion

Liên kết giữa kim loại với phi kim điển hình
=> Liên kết ion
=> Đáp án C

Đáp án B
X có 1 electron lớp ngoài cùng, electron cuối cùng điền vào phân lớp 4s
→ X thuộc chu kì 4, nhóm IA.
X có xu hướng dễ dàng nhường 1 electron để tạo thành ion: X → X+ + 1e.
Y có 7 electron lớp ngoài cùng, electron cuối cùng điền vào phân lớp 2p
→ Y thuộc chu kì 2, nhóm VIIA.
Y có xu hướng dễ dàng nhận 1 electron để tạo thành ion: Y + 1e → Y-.
Hai ion được tạo thành mang điện tích ngược dấu hút nhau bằng lực hút tĩnh điện, tạo nên phân tử XY: X+ + Y- → XY.

Chọn A
X có 1 e lớp ngoài cùng do đó X là kim loại điển hình.
Y có 7 e lớp ngoài cùng do đó Y là phi kim điển hình.
Vậy liên kết giữa nguyên tử X và Y là liên kết ion.
Đáp án D
Cấu hình e của X: , Vậy X là Clo (độ âm điện 3,16)
, Vậy X là Clo (độ âm điện 3,16)
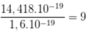
Số p trong Y:
Suy ra, Y là Flo (độ âm điện 3,98)
HIệu độ âm điện: 3,98-3,16=0,82 nên liên kết giữa 2 ng tử này là cộng hóa trị có cực